
| A | B | C | D |
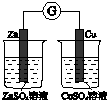 | 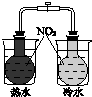 | 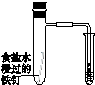 | 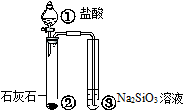 |
| 验证化学能 转化为电能 | 证明温度 对平衡移动的影响 | 验证铁 发生析氢腐蚀 | 验证H2CO3的酸性大于H2SiO3 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| 白色粉末的成分 | 形成的原因 |
| 可能是CaCO3. | |
| 可能是 | 暑假气温较高,溶质的溶解度降低或溶剂蒸发,石灰水中的溶质结晶析出. |
| OH- | Cl- | CO32- | NO3- | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
| 实 验 步 骤 | 可能观察到的现象 | 结 论 |
| 取上述试管中的上层清液,滴加1~2酚酞试液. | ||
| 往上述试管中残留的固体中加入稀盐酸. | 白色粉末中 (选填“有”或“无”)CaCO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单位时间生成3nmolA2的同时生成nmolB2 |
| B、c(A2):c(B2):c(C)=3:1:4 |
| C、单位时间生成4nmolC的同时生成nmolB2 |
| D、混合气体的压强不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
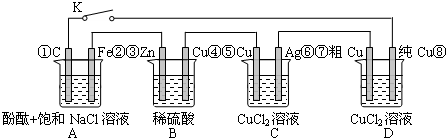
| A、当K闭合时,A装置发生吸氧腐蚀,在电路中做电源 |
| B、当K断开时,B装置锌片溶解,有氢气产生 |
| C、当K闭合后,整个电路中电子的流动方向为①→⑧;⑦→⑥;⑤→④;③→② |
| D、当K闭合后,A、B、C、D装置中pH均变大. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它们都是酸,因此彼此不发生反应 |
| B、只有亚硫酸可以露置在空气中,其他酸都不行 |
| C、鉴别三种酸溶液时,只要分别滴入BaCl2溶液即可 |
| D、它们是二元酸,酸性H2S<H2SO3<H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若x=2,则p>0.5a |
| B、若x=3,则p>0.7a |
| C、若x=4,则p=a |
| D、若x=5,则p≥a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| C、SO2具有氧化性,可用于漂白纸浆 |
| D、苏打显碱性,可用作面碱,防止面粉发酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com