
| A、Na+、Mg2+、SO42-、OH- |
| B、Ba2+、K+、SO42-、NO3- |
| C、H+、K+、Cl-、HCO3- |
| D、Fe3+、K+、SO42-、Cl- |
科目:高中化学 来源: 题型:
 同学们为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,他们准备了以下化学用品:0.2mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
同学们为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,他们准备了以下化学用品:0.2mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.| 实验 编号 |
温度(K) | 盐酸浓度 (mol?L-1) |
醋酸浓度(mol?L-1) | 实验目的 |
| ① | 298 | 0.20 | / | a.实验①和②是探究 b.实验①和③是探究 c.实验①和④是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别. |
| ② | 308 | 0.20 | / | |
| ③ | 298 | 0.40 | / | |
| ④ | 0.20 | / |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
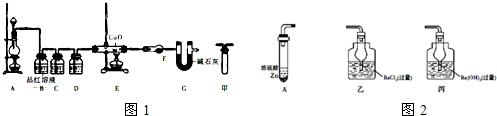
查看答案和解析>>
科目:高中化学 来源: 题型:
A、向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-
| ||||||
B、用银氨溶液检验乙醛的醛基:CH3CHO+2Ag(NH3
| ||||||
C、向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O-→2C6H5OH+2C
| ||||||
| D、甘氨酸(H2N-CH2-COOH)与氢氧化钠溶液反应:H2N-CH2-COOH+OH-→H2N-CH2COO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4 g重水(D2O)中所含中子数为0.2NA |
| B、4.48 L H2和O2的混合气体中所含分子数为0.2NA |
| C、0.2 mol Cl2溶解于等体积的水中,转移电子数为0.2NA |
D、12.6 g三聚氰胺(结构如右图)所含碳氮单键的数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)已知:N≡N的键能是946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,请根据此次而出合成氨反应的热化学方程式
(1)已知:N≡N的键能是946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,请根据此次而出合成氨反应的热化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、交警查酒驾的装置中K2Cr2O4与酒精反应时,K2Cr2O4被酒精氧化了 |
| B、甲醛可用于配制消毒液是由于其具有强氧化性 |
| C、在一定条件下能发生反应:Cu+2HCl═CuCl2+H2↑ |
| D、化工上可用氨气检验氯气是否泄漏,若泄漏则产生白烟现象,该反应中还原产物只有HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com