
甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路,质子经内电路到达另一极与氧气反应,电池总反应式为2CH3OH+3O2 2CO2+4H2O。下列关于该电池的分析:①甲醇是负极②H+向负极移动③负极反应:CH3OH-6e-+H2O=CO2+6H+ ④1 mol CH3OH完全反应转移12 mol电子 ⑤正极反应:O2+4e-+2H2O==4OH- ⑥该电池的电解质溶液可能是碱液。其中正确的是
2CO2+4H2O。下列关于该电池的分析:①甲醇是负极②H+向负极移动③负极反应:CH3OH-6e-+H2O=CO2+6H+ ④1 mol CH3OH完全反应转移12 mol电子 ⑤正极反应:O2+4e-+2H2O==4OH- ⑥该电池的电解质溶液可能是碱液。其中正确的是
A.①②⑥ B.②③④⑤ C.③ D.①③
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如2Fe3+ + Cu ==2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e- ==Cu2+,还原反应式:2Fe3+ + 2e- ="=" 2Fe2+。并由此实现了化学能与电能的相互转化。据此,回答下列问题:
(1)将反应Zn + 2H+ = Zn2+ + H2↑拆写为两个“半反应式”:其中,氧化反应为: 。
(2)由题(1)反应,设计成原电池如图所示:
若电极a为Zn ,电极b可选择材料: (只填一种);电解质溶液甲是 ;电极b处的电极反应式: 。
(3)由反应2H2 + O2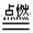 2H2O ,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极 ,正极 。
2H2O ,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极 ,正极 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作不能达成实验目的的是( )
A.溴乙烷与氢氧化钠溶液共煮后,加入硝酸银检验Br-
B.用电石和饱和食盐水制取乙炔
C.用苯、2mol/L的硝酸制硝基苯
D.用四氯化碳萃取碘水中的碘
查看答案和解析>>
科目:高中化学 来源: 题型:
两种微粒含有相同的质子数和电子数,这两种微粒的关系可能是:(1)同一元素的不同原子,(2)不同元素的原子,(3)两种不同的分子,(4)一种原子和一种分子,(5)一种原子和一种离子,(6)一种分子和一种离子,(7)两种不同的阳离子,(8)两种不同的阴离子,(9)一种阴离子和一种阳离子,其中正确的是
A.(1)(3)(4)(7)(8) B.(1)(2)(5)(7)(9) C.(1)(2)(5)(7)(9) D.(1)(2)(3)(4)(5)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的用途,说法不正确的是
A.甲烷是一种热量高、污染小的清洁能源
B.乙烯最重要的用途是作为植物生长调节剂
C.乙醇是一种很好的溶剂,能溶解多种有机物和无机物
D.酯类物质常用作饮料、糖果、香水、化妆品中的香料
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3+5O2 4NO+6H2O在5 L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率表达正确的是
4NO+6H2O在5 L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率表达正确的是
A.v(O2)=0.01mol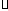 L-1
L-1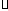 s-1 B.v(NO)=0.008 mol
s-1 B.v(NO)=0.008 mol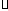 L-1
L-1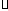 s-1
s-1
C.v(H2O)=0.003 mol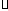 L-1
L-1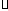 s-1 D.v(NH3)=0.004 mol
s-1 D.v(NH3)=0.004 mol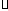 L-1
L-1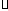 s-1
s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。主要实验步骤如下:
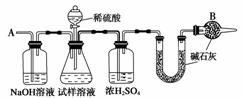
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U形管的质量,为b g
④从分液漏斗滴入6 mol·L-1的稀硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U形管的质量,为c g
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明______________。
(2)装置中干燥管B的作用是____________。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果________(填“偏高”、“偏低”或“不变”)。
(4)步骤⑤的目的是__________________。
(5)步骤⑦的目的是__________________。
(6)该试样中纯碱的质量分数的计算式为____________________________________
(用含a、b、d的代数式表示)。
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验方法。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com