
| A. | 制备Al(OH)3悬浊液:向1mol•L-1AlCl3溶液中加过量的6mol•L-1NaOH溶液 | |
| B. | 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量15%的Na2CO3溶液,振荡后静置分液,并除去有机相的水 | |
| C. | 检验溶液中是否含有Fe2+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象 | |
| D. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
分析 A.NaOH过量,反应生成偏铝酸钠;
B.乙酸与碳酸钠反应后,与乙酸乙酯分层;
C.加入少量新制氯水了氧化亚铁离子;
D.相同条件下,只有催化剂不同.
解答 解:A.NaOH过量,反应生成偏铝酸钠,不能制备Al(OH)3悬浊液,故A错误;
B.乙酸与碳酸钠反应后,与乙酸乙酯分层,则振荡后静置分液,并除去有机相的水,故B正确;
C.加入少量新制氯水了氧化亚铁离子,检验亚铁离子,应先加KSCN溶液,再加氯水,故C错误;
D.相同条件下,只有催化剂不同,试管中加入2mL5%H2O2和1mLFeCl3溶液反应速率快,则可探究催化剂对H2O2分解速率的影响,故D正确;
故选BD.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的性质、混合物分离提纯、离子检验及影响反应速率的因素等,把握物质的性质及反应原理为解答的关键,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
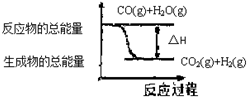
| A. | 依图象可知反应:CO(g)+H2O(g)?CO2(g)+H2(g) | |
| B. | 无法判断反应物总能量与生成物总能量的相对大小 | |
| C. | 表示此反应是吸热反应 | |
| D. | 此反应:△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol N2 的质量是14g | B. | H2SO4的摩尔质量是98 g | ||
| C. | H2O的摩尔质量是18 g/mol | D. | 1mol HCl的质量是36.5 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
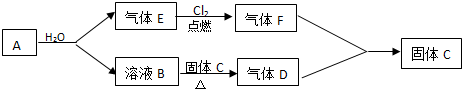
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式: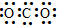 | B. | 碳原子最外层电子的轨道表示式: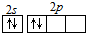 | ||
| C. | 淀粉分子的最简式:CH2O | D. | 乙烯分子的比例模型 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸反应 C032-+2H+═C02↑+H20 | |
| B. | KI溶液中通氯气 2Iˉ+C12═2C1?+I2 | |
| C. | 氯气通入氯化亚铁溶液中:Fe2++Cl2═Fe3++2Cl- | |
| D. | 硫酸与氢氧化钡溶液反应 H十+OHˉ═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | c(HA)/mol•L-1 | c(NaOH)/mol•L-1 | 反应后溶液pH |
| 甲 | 0.1 | 0.1 | pH=9 |
| 乙 | c1 | 0.2 | pH=7 |
| A. | 0.1mol•L-1的HA溶液中由水电离出的c(H+)>1×10-13mol/L | |
| B. | c1一定大于0.2 mol•L-1 | |
| C. | 甲反应后的溶液中:HA占含A-微粒总数的0.01% | |
| D. | 乙反应后的溶液中:c(Na+)<c(HA)+c(A-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com