
| ���� | Na+ | Mg2+ | Cl- | SO42- |
| Ũ��/��g•L-1�� | 63.7 | 28.8 | 144.6 | 46.4 |
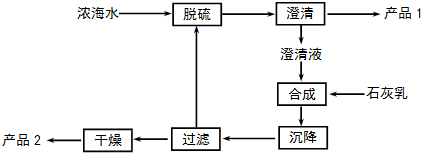
���� ��1��������ʹ���������ʺͽ���ۼ��ɽϴ�ŵĿ�����������Ȼ����˳�ȥ�����ܽ��к�ˮ������ͨ���ı乤�գ�������߲��ֲ�Ʒ���������Ż���ȡ��Ʒ��Ʒ�֣����Ը��ݲ�ͬ��ԭ���Ľ��ء��塢þ�ȵ���ȡ���գ�
��2����Ũ��ˮ����Br2�����ô������գ����绯ΪBr-��BrO3-��û�в���CO2��Ӧ����̼�����ƣ�
��3���������̺ϳɲ����м���ʯ���飬���������˺����Һ��������Ӧ���ø����ӳ��������������������Ƴ�������Ʒ1Ϊ����ƣ��ϳɵõ�������þ�������ʹ��˺����IJ�Ʒ2Ϊ������þ������1L��Һ��Mg2+������������Mg2+��Mg��OH��2����������þ��������
��4�����ʱ����������ˮ���ڣ�Mg��ˮ��Ӧ����������þ������������ɲ�Ʒþ�����ģ�
��� �⣺��1���ٻ������Ǽ���һ�ֻ��������磺���������εȣ���ʹˮ��ϸС���������ʺͽ���ۼ��ɽϴ�ŵĿ�����������Ȼ����˳�ȥ����ˮ�п��������ʲ��ܳ�ȥ�����ܽ��к�ˮ�������ʢٴ���
�ڸĽ����գ������ܼ������������룬��ȥ�ֲ�Ʒ�е����ʣ�������߲�Ʒ���������ʢ���ȷ��
�ۺ�����һ��Զδ��ȫ�����ľ�ѧ��Դ���⣬��ˮ��Ԫ������ܶ࣬�Ľ����տ����Ż���ȡ��Ʒ��Ʒ�֣��ʢ���ȷ��
�ܸ��ݲ�ͬ����ȡԭ�����ԸĽ��ء��塢þ�ȵ���ȡ���գ��Ӷ����K��Br2��Mg�ȵ���ȡ�������ʢ���ȷ��
��ѡ���ڢۢܣ�
��2����Ũ��ˮ����Br2�����ô������գ����绯ΪBr-��BrO3-��û�в���CO2��Ӧ����̼�����ƣ���Ӧ�����ӷ���ʽΪ��3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3-��
�ʴ�Ϊ��3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3-��
��3���������̺ϳɲ����м���ʯ���飬���������˺����Һ����������Ca2+����SO42-����CaSO4���������ӷ���ʽΪ��Ca2++SO42-=CaSO4�������ù��˵ķ����õ���Ʒ1ΪCaSO4����Һ�м���ʯ���飬������ӦΪMg2+��aq��+Ca��OH��2��s��=Mg��OH��2��s��+Ca2+ ��aq�����ϳ���Ӧ�õ�Mg��OH��2���������ˡ�����IJ�Ʒ2ΪMg��OH��2��Ũ��ˮ��������Ϊ90%
��Һ��m��Mg2+��=1L��90%��28.8g/L=25.92g��
Mg2+��Mg��OH��2
24g 58g
25.92g m[Mg��OH��2]
m[Mg��OH��2]=25.92g��$\frac{58g}{24g}$=62.64g��
�ʴ�Ϊ��Ca2+��Mg2+��aq��+Ca��OH��2��s��=Mg��OH��2��s��+Ca2+ ��aq����62.64��
��4�����ʱ����������ˮ���ڣ�Mg��ˮ��Ӧ����������þ������������ɲ�Ʒþ�����ģ���Ӧ����ʽΪ��Mg+2H2O$\frac{\underline{\;����\;}}{\;}$Mg��OH��2+H2������HCl�������Χ�м��ȣ�����MgCl2ˮ�⣻
�ʴ�Ϊ������MgCl2ˮ�⣮
���� ���⿼�麣ˮ��Դ�������á�������ԭ��Ӧ���㡢���ԭ����֪ʶ���Ի���֪ʶ�ܽ����ۺ������ǽ��ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
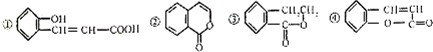
| A�� | ֻ�Т��ܺ�̼���Ʒ�Ӧ�ų����� | B�� | �ںܻ͢�Ϊͬ���칹�� | ||
| C�� | �٢ڢܶ�����ʹ��ˮ��ɫ | D�� | ����H2�ӳɺ���Եõ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
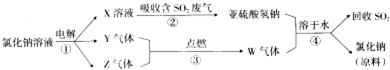
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6�� | B�� | 8�� | C�� | 10�� | D�� | 12�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ũ������±�� | B�� | ��Ũ���Ṳ����ȥ | ||
| C�� | ͭ������ | D�� | ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
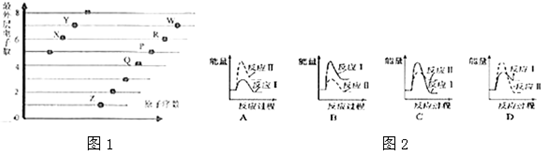
| A�� | 25��ʱ0.1mol/LX2W��Һ��pH��1-lg2 | |
| B�� | ��Һ��ˮ�ĵ���̶ȣ�RYX��R2W | |
| C�� | ���ȶ��ԣ�X2Y��X2W | |
| D�� | ��X��Y��Z��W��R����Ԫ����ɵ�һ�ֻ����������ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 2��5 | C�� | 3��4 | D�� | 5��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 30.8% | B�� | 28.6% | C�� | 25.3% | D�� | 22.7% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com