
�����������������ڴ��������еĵ�����������Ļ�ѧ��ӦΪ��
2NH3(g)��NO(g)��NO2(g)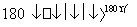 2N2(g)��3H2O(g)����H<0
2N2(g)��3H2O(g)����H<0
�ں��ݵ��ܱ������У������й�˵����ȷ����(����)
A��ƽ��ʱ�������������䣬�����¶ȿ�ʹ�÷�Ӧ��ƽ�ⳣ������
B��ƽ��ʱ�������������䣬����NH3��Ũ�ȣ������е��������ת���ʼ�С
C����λʱ��������NO��N2�����ʵ�����Ϊ12ʱ����Ӧ�ﵽƽ��
D�������������䣬ʹ�ø�Ч�����������е��������ת��������
 �п������п��Ծ����ϵ�д�
�п������п��Ծ����ϵ�д� ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��20����������������Ϊδ���Ķ���ȼ������Դ���о������Ѹ�ٷ�չ�����һ��������һ����Ҫ����������Դ��ʯ�͡�ú��ԭ���ܵȵ���������ȡ����ν��������Դ��������������Ȼ��Ŀ����ṩ�ֳ���ʽ��������Դ��Ϊһ����Դ����ú��ʯ�͡�̫���ܺ�ԭ���ܵȡ�
(1)Ϊ����Ч��չ��������Դ�����ȱ����Ƶ����۵����������пɹ������ֽϾ�����ԭ�Ͽɳ������õ��������ķ�����(����)
A�����ˮ B��п��ϡ���ᷴӦ
C����⺣ˮ D����ʯ�͡���Ȼ��Ϊԭ��
(2)����ȼ��ʱ������С������������֪�����Ȼ�ѧ����ʽ��C(g)��O2(g)===CO2(g)
��H����393.5 kJ·mol��1��H2(g)��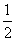 O2(g)===H2O(l)����H����285.8 kJ·mol��1
O2(g)===H2O(l)����H����285.8 kJ·mol��1
��ͨ������˵����������������̼ȼ��ʱ���������ı���____________________________________________________��
(3)����Դ�п���ʵ����Դ�����棬Ҳ�п���ʵ�־��á���Ч�����͡��о��������ɽ������⻯��(�ֳƼ���⻯��)���������⻯���У���ԭ������ڽ����ľ����϶֮�䣬����ɲ��̶���ͨ���Ƿǻ�ѧ�����ģ��磺LaH2.76��TiH1.73��CeH2.69��ZrH1.98��PrH2.65��TaH0.78����֪��״���£�1������ٷ۴�Լ������896���������(�ٷ۵��ܶ�Ϊ10.64 g/cm3�����ԭ������Ϊ106.4)����д����(Pd)���⻯��Ļ�ѧʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
0.1 molij����1.5 mol����������ϣ����ȼ�պ�������ȫ��ͨ��������Na2O2���壬��������23.4 g����Na2O2���ݳ���״����24.64 L���塣
(1)������ķ���ʽ��
(2)��֪������ʹKMnO4������Һ��ɫ��������ʹ��ˮ��Ӧ��ɫ��д���������ܵĽṹ��ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶�ʱ�����0.01 mol·L��1��NaOH��Һ��pHΪ11������¶���ˮ�����ӻ�����Ϊ________________��
�ڴ��¶��£���pH��a��H2SO4��ҺVaL��pH��b��NaOH��ҺVbL��ϡ�
(1)�����û��ҺΪ���ԣ���a��2��b��12����VaVb��________��
(2)�����û��Һ��pH��10����a��2��b��12����VaVb��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ı仯����Ϊ���ͻ�ܣ����ӵ�λ����ڷ�Ӧ������л���ӵİٷ�����ʹ��Ӧ���ʼӿ����(����)
A������Ũ�� B������ѹǿ
C�������¶� D��ʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶��£�H2(g)��CO2(g)H2O(g)��CO(g)��ƽ�ⳣ��K��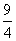 �����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�����±���ʾ��
�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�����±���ʾ��
| ��ʼŨ�� | �� | �� | �� |
| c(H2)(mol·L��1) | 0.010 | 0.020 | 0.020 |
| c(CO2)(mol·L��1) | 0.010 | 0.010 | 0.020 |
�����жϲ���ȷ����(����)
A��ƽ��ʱ������CO2��ת���ʴ���60%
B��ƽ��ʱ�����кͱ���H2��ת���ʾ���60%
C��ƽ��ʱ������c(CO2)�Ǽ��е�2������0.012 mol·L��1
D����Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
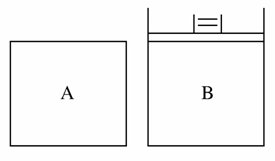
��A��B������(��ͼ��ʾ)��A�ݻ��̶���B�ݻ��ɱ䡣һ���¶��£���A�м�2 mol N2��3 mol H2��������Ӧ��N2��3H22NH3����ƽ��ʱ����NH3�����ʵ���Ϊn��
(1)��ͬ�¶��£���B�г���4 mol N2��6 mol H2����B��ѹǿ��A��ѹǿ��ȣ�B�з�Ӧ��ƽ��ʱ������NH3�����ʵ���________2n(�>����<����������ͬ)����B���ݻ���A���ݻ���ȣ�B�з�Ӧ��ƽ��ʱ������NH3�����ʵ���________2n��
(2)��ͬ�¶��£�����B���ݻ�ΪA��һ�룬������1 mol NH3��ҪʹB�з�Ӧ��ƽ��ʱ�����ʵ�Ũ�ȷֱ�������A������ƽ��ʱ��ͬ������ʼʱӦ����________mol N2��________mol H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��װ�ý���ʵ�飬��ͼ�к�����x��ʾͨ���缫�ĵ��ӵ����ʵ���������������ȷ����(����)
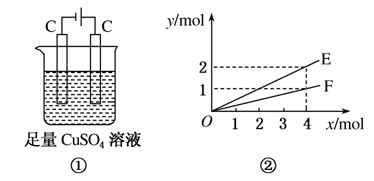
A��F��ʾ��Ӧ����Cu�����ʵ���
B��E��ʾ��Ӧʵ������H2O�����ʵ���
C��E��ʾ��Ӧ����O2�����ʵ���
D��F��ʾ��Ӧ����H2SO4�����ʵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ý��������۽��͵��� (����)��
A�������� B��������
C����չ�� D����ʴ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com