
【题目】氨气在生产、生活和科研中应用十分广泛。
(1)①SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),SNCR-SCR流程中发生的主要反应有:
4NO(g)+4NH3(g)+O2(g) ![]() 4N2(g)+6H2O(g)△H=-1627.2kJmol-1;
4N2(g)+6H2O(g)△H=-1627.2kJmol-1;
6NO(g)+4NH3(g) ![]() 5N2(g)+6H2O(g)△H=-1807.0kJmol-1;
5N2(g)+6H2O(g)△H=-1807.0kJmol-1;
6NO2(g)+8NH3(g) ![]() 7N2(g)+12H2O(g)△H=-2659.9kJmol-1;
7N2(g)+12H2O(g)△H=-2659.9kJmol-1;
反应N2(g)+O2(g) ![]() 2NO(g)的△H= ____________ kJmol-1
2NO(g)的△H= ____________ kJmol-1
②液氨可以发生电离:2NH3(l) ![]() NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式____________;
NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式____________;
(2)氨气易液化,便于储运①若在恒温恒容的容器内进行反应2NH3(g) ![]() N2(g)+3H2(g);△H=+94.4kJ/mol,下列表示该反应达到平衡状态的标志有____________(填字母序号)
N2(g)+3H2(g);△H=+94.4kJ/mol,下列表示该反应达到平衡状态的标志有____________(填字母序号)
A.容器中混合气体的密度保持不变
B.NH3(g)百分含量保持不变
C.容器中混合气体的压强保持不变
D.有3个H-H键生成同时又1个N≡N键生成
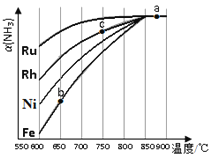
②其他条件相同时,该反应在不同催化剂作用下反应,相同时间后,氨气的转化率随反应温度的变化如图所示.在600℃时催化效果最好的是____________(填催化剂的化学式).c点氨气的转化率高于b点,原因是____________。
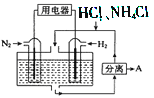
(3)如图表示使用新型电极材料,以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池。请写出该电池的正极反应式____________;生产中可分离出的物质A的化学式为____________。
【答案】
(1)①+179.8;
②COCl2+4NH3=CO(NH2)2+2NH4Cl;
(2)①BC
②Ru;c点温度较高,且Ru比Fe的催化能力更强
(3)N2+8H++6e-═2NH4+;NH4Cl。
【解析】
试题分析:(1)①4NO(g)+4NH3(g)+O2(g)![]() 4N2(g)+6H2O(g)△H=-1627.2kJmol-1;②6NO(g)+4NH3(g)
4N2(g)+6H2O(g)△H=-1627.2kJmol-1;②6NO(g)+4NH3(g)![]() 5N2(g)+6H2O(g)△H=-1807.0kJmol-1;③6NO2(g)+8NH3(g)
5N2(g)+6H2O(g)△H=-1807.0kJmol-1;③6NO2(g)+8NH3(g)![]() 7N2(g)+12H2O(g)△H=-2659.9kJmol-1;依据盖斯定律①-②得到N2(g)+O2(g)
7N2(g)+12H2O(g)△H=-2659.9kJmol-1;依据盖斯定律①-②得到N2(g)+O2(g)![]() 2NO(g)△H=+179.8kJmol-1;故答案为:+179.8;
2NO(g)△H=+179.8kJmol-1;故答案为:+179.8;
②由于液氨的电离方程式为2NH3(l)![]() NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,而尿素的化学式为CO(NH2)2,可知该反应的化学方程式为COCl2+4NH3=CO(NH2)2+2NH4Cl,故答案为:COCl2+4NH3=CO(NH2)2+2NH4Cl;
NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,而尿素的化学式为CO(NH2)2,可知该反应的化学方程式为COCl2+4NH3=CO(NH2)2+2NH4Cl,故答案为:COCl2+4NH3=CO(NH2)2+2NH4Cl;
(2)①若在恒温恒容的容器内进行反应2NH3(g) ![]() N2(g)+3H2(g);△H=+94.4kJ/mol。A.容器中混合气体的密度始终保持不变,不能表示该反应达到平衡状态的标志,故A错误;B.NH3(g)百分含量保持不变,表示该反应达到平衡状态的标志,故B正确;C.该反应属于气体的物质的量发生变化的反应,容器中混合气体的压强保持不变,表示该反应达到平衡状态的标志,故C正确;D.有3个H-H键生成同时必定有1个N≡N键生成,不能表示该反应达到平衡状态的标志,故D错误;故选BC。
N2(g)+3H2(g);△H=+94.4kJ/mol。A.容器中混合气体的密度始终保持不变,不能表示该反应达到平衡状态的标志,故A错误;B.NH3(g)百分含量保持不变,表示该反应达到平衡状态的标志,故B正确;C.该反应属于气体的物质的量发生变化的反应,容器中混合气体的压强保持不变,表示该反应达到平衡状态的标志,故C正确;D.有3个H-H键生成同时必定有1个N≡N键生成,不能表示该反应达到平衡状态的标志,故D错误;故选BC。
②根据图可知,在600℃时催化效果最好的是Ru,b、c点均未达到平衡,c点温度较高,反应速率较快,氨气的转化率较高,故答案为:Ru;c点温度较高,且Ru比Fe的催化能力更强;
(3)放电过程中,负极电极反应为:H2-2e-=2H+,正极电极反应N2+8H++6e-═2NH4+;生产中可分离出的物质A的化学式为NH4Cl,故答案为:N2+8H++6e-═2NH4+;NH4Cl。


科目:高中化学 来源: 题型:
【题目】苯甲酸钠(![]() ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A-。已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.17×10-7,Ka2=4.90×10-11,在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)
,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的抑菌能力显著高于A-。已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.17×10-7,Ka2=4.90×10-11,在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)
A.相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B.提高CO2充气压力,饮料中c(A-)不变
C.当pH为5.0时,饮料中![]() =0.16
=0.16
D.碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO3-)+c(CO32-)+c(OH-)-c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
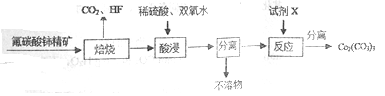
【题目】碳酸铈[Ce2(CO3)3]为白色粉末,难溶于水,主要用作生产铈的中间化合物。它可由氟碳酸铈精矿经如下流程制得。
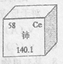
(1)如图是一种稀土元素铈(Ce)在元素周期表中的信息示意图。则铈原子的质子数是______,氟碳酸铈的化学式为CeFCO3,该化合物中,Ce的化合价为_____________;
(2)焙烧生成的铈化合物为二氧化铈(CeO2),其在酸浸时发生反应的离子方程式为______________;
(3)试剂X______________;
(4)已知298K时,Ksp[Ce(OH)4]=1×10-29,Ce(OH)4的溶度积表达式为Ksp=______________;为了使溶液中Ce4+沉淀完全,需调节pH为________以上;
(5)取某Ce(OH)4产品1.00g(质量分数为97%),加硫酸溶解后,用0.1000molL-1的FeSO4溶液滴定至终点(铈被还原成Ce3+)则需要滴加标准溶液的体积____________mL,若用硫酸酸化后改用0.1000molL-1
的FeCl2溶液滴定产品从而测定Ce(OH)4产品的质量分数,其它操作都正确,则测定的Ce(OH)4产品的质量分数__________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A.徐光宪建立稀土串级萃取理论
B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发重油裂解催化剂
D.侯德榜联合制碱法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有关物质的叙述正确的是( )
①酸性氧化物肯定是非金属氧化物 ②不能跟酸反应的氧化物一定能跟碱反应 ③碱性氧化物肯定是金属氧化物 ④分散系一定是混合物 ⑤浊液均可用过滤的方法分离
A.①③ B.③④ C.②④ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请将符合题意的下列变化的序号填在对应的横线上:①碘的升华;②氧气溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解.
(1)化学键没有被破坏的是 ;
(2)仅发生离子键破坏的是 ;
(3)仅发生共价键破坏的是 ;
(4)既发生离子键又发生共价键破坏的是 ;
(5)已知拆开1mol H﹣H键、1mol N≡N、1mol N﹣H键分别需要吸收的能量为436kJ、946k J、391k J.则由N2和H2反应生成1mol NH3需要放出 的热量.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
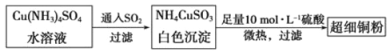
①Cu2+的价电子排布图 ;NH4CuSO3中N、O、S三种元素的第一电离能由大到小顺序为________(填元素符号)。
②SO42-的空间构型为 ,SO32-离子中心原子的杂化方式为 。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式 。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因 。
(4)Cu晶体的堆积方式如图所示,设Cu原子半径为r,晶体中Cu原子的配位数为 ,晶体的空间利用率为 (列式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
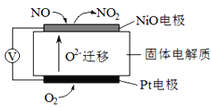
【题目】2015年9月爆发的德国大众车尾气排放作弊事件引起了公众的关注。大众车尾气中常含有大里氮氧化物.通常会采用喷射尿素溶液的方法,将有毒的氮氧化物还原成无污染的物质。大众选择了一种违规做法,即在客户平时用车时不开启喷射尿素的尾气后处理系统,而是通过软件让这一系统只在尾气排放检测时启动。
I、通过NOx传感器可监测空气的NOx的含量,其工作原理图如下图,写出NiO电极的电极反应式__________________;
Ⅱ、以CO2与NH3为原料可合成尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-l59.5kJmol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5kJmol-1
③H2O(l)=H2O(g) △H=+44.0kJmol-1
(1)写出CO2与NH3合成尿素和液态水的热化学反应方程式____________;
(2)恒温下将2molNH3和1molCO2放入容积为2L的密闭容器中,反应生成NH2CO2NH4(s),2分钟后达到平衡。此时NH3的浓度为0.8mol/L,则CO2的反应速率为________,NH3的转化率是________。
Ⅲ、尿素在一定温度下可分解生成NH3,NH3催化还原NxOy可以消除氮氧化物的污染。已知:
反应a:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l)
5N2(g)+6H2O(l)
反应b:2NO(g)+O2(g)![]() 2NO2(g)
2NO2(g)
反应c: 4NH3(g)+6NO2(g)![]() 5N2(g)+3O2(g)+6H2O(l)
5N2(g)+3O2(g)+6H2O(l)
(1)相同条件下,反应a在2L密闭容器内,选用不同的催化剂,反应产物N2的量随时间变化如图所示。下列说法正确的是________________。
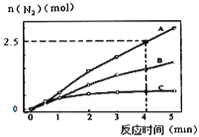
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
(2)对于反应c来说,可加快反应速率的措施有_______________(任写2种)
(3)恒温恒容条件下,反应b达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2,在其他条件不变时,再充入NO2气体,NO2体积分数_______(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
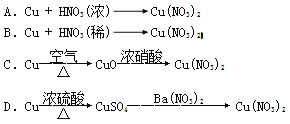
【题目】 I.工业上用洗净的废铜屑作原料来制备硝酸铜。为了节约原料和防止污染环境,宜采取的方法是 (填序号)
Ⅱ.下图是用过量的铜与40mL稀硝酸在100mL烧瓶中反应制取一氧化氮气体的实验装置图,请回答下列问题:
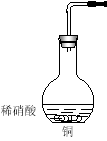

(1)请在右框中画出气体收集装置的装置图。
(2)①从烧瓶中取出少量反应后的溶液,滴入少量氨水,写出该反应的离子方程式: _______________
②反应结束后,能否采取向烧瓶中再加入稀硫酸的方式,再获得一氧化氮气体?如果可以,请写出反应的离子方程式,如果不可以,请说明理由:_________________________________
(3)检查上图装置气密性的操作是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com