
| A. | 升温 | B. | 减小气体压强 | ||
| C. | 增大反应物的浓度 | D. | 使用催化剂 |
分析 增大压强、浓度,单位体积活化分子的数目增多,不改变活化分子百分数,升高温度、加入催化剂活化分子的百分数增大,能发生化学反应的碰撞是有效碰撞,以此解答.
解答 解;A.升高温度活化分子的百分数增大,故A不选;
B.减小压强,单位体积活化分子的数目减小,不改变活化分子百分数,故B不选;
C.增大反应物的浓度单位体积内活化分子数增大,但不改变活化分子百分数,故C选;
D.使用催化剂活化分子的百分数增大,故D不选.
故选C.
点评 本题考查影响活化分子的因素,为高频考点,侧重于学生的分析能力的考查,注意相关知识的积累,学习中注意温度、浓度、压强、催化剂对反应速率的影响的根本原因是影响活化分子的浓度或百分数,难度不大.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 硫酸铵稀溶液和稀氢氧化钡溶液反应:NH4++SO42-+Ba2++OH-═BaSO4↓+NH3•H2O | |
| C. | 把氯气通入NaOH 溶液中:Cl2+2OH-═Cl-+ClO-+2H2O | |
| D. | 碳酸氢钙溶液中加入少量的氢氧化钠:Ca2++HCO3-+OH-═H2O+CaCO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
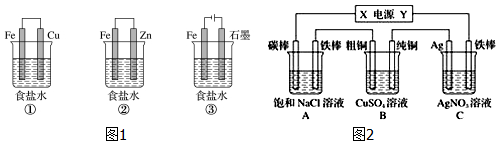
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20 mL 2 mol/L 的X溶液 | B. | 10 mL 4 mol/L 的X溶液 | ||
| C. | 20 mL 3 mol/L 的X溶液 | D. | 10 mL 2 mol/L 的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应属于复分解反应 | |
| B. | 氧化性:KBrO3<KClO3 | |
| C. | 反应中氧化剂与还原剂的物质的量之比为1:2 | |
| D. | 反应中若有1mol还原剂发生反应,则氧化剂得到10mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3溶液中:K+、Na+、SO42-、SCN- | |
| B. | 加入金属铝后溶液中有大量气泡产生的溶液中:Fe2+、Mg2+、NO3-、Cl- | |
| C. | 漂白粉溶液中:K+、Na+、I-、CO32- | |
| D. | 在强碱性溶液中能大量存在:Na+、K+、Cl-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁具有良好的导电性,氯碱工业中可用铁作阳极电解食盐水 | |
| B. | 药皂中加入少量苯酚,可以起到杀菌消毒的作用 | |
| C. | 铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| D. | 氯化铝是一种电解质,可用于电解法制铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com