
| 46.2KJ/ |
| 92.4KJ/mol |
| 0.5mol |
| 2mol |
| 1mol |
| 2mol+4mol-1mol |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ԭˮ����ȵ��ˮ��������ܻ����������� |
| B��������ˮ����NH4+��NH3�����û�ѧ��������绯ѧ���������� |
| C��ij�ֹ�ѧ��⼼�����м��ߵ������ȣ��ɼ�����ϸ����V��10-12L���ڵ�����Ŀ����ӣ��ݴ˿�����ü�⼼���ܼ��ϸ����Ũ��ԼΪ10-12-10-11mol?L-1��Ŀ����� |
| D�������������Ӽ״��û��ȼ�ϵ���ֵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
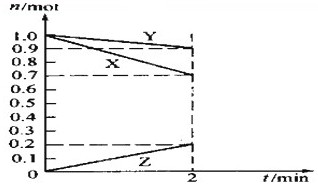
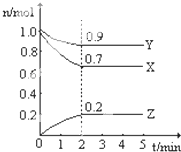 I��ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�
I��ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�| ʵ����� | �Ȼ�þ��������Ԫ�غ���/% | �¶�/�� | ���鷽ʽ/ | ��Ч��/g?g-1 |
| 1 | 70.97 | 20 | ������ĥ | 3.9��104 |
| 2 | 74.45 | 20 | ������ĥ | 5.0��104 |
| 3 | 74.45 | 20 | ����ĥ | 5.9��104 |
| 4 | �� | 100 | ����ĥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
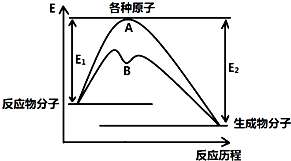 ��֪ij��Ӧ�ڲ�ͬ�����µķ�Ӧ���̿��Ա�ʾ����ͼ��ʾ��E1��ʾ��Ӧ����ӱ��ԭ�������յ�������E2��ʾ��Щԭ�����³ɼ��γ�������ų�����������ش��������⣺
��֪ij��Ӧ�ڲ�ͬ�����µķ�Ӧ���̿��Ա�ʾ����ͼ��ʾ��E1��ʾ��Ӧ����ӱ��ԭ�������յ�������E2��ʾ��Щԭ�����³ɼ��γ�������ų�����������ش��������⣺| ��ѧ�� | H-H | Cl-Cl | O=O | O-H | H-Cl |
| ���ܣ�kJ?mol-1�� | 436 | 247 | x | 463 | 431 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
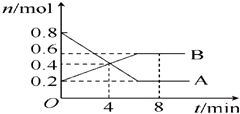
 ��1����ӦA+3B=2C+2D�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ
��1����ӦA+3B=2C+2D�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com