
| A. | c(Na+)=2c(S2-)+2c(HS-)+2c(H2S) | B. | c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) | ||
| C. | c(Na+)>c(S2-)>c(OH-)>c(HS-) | D. | c(OH-)=c(H+)+c(HS-)+c(H2S) |
分析 在Na2S溶液中,硫离子易水解,钠离子不水解,且硫离子的第一步水解程度大于第二步,根据电荷守恒、物料守恒来分析解答.
解答 解:A.根据物料守恒知,C(Na+)=2c(HS-)+2c(S2-)+2c(H2S),故A正确;
B.溶液呈电中性,所以阴阳离子所带电荷相等,即c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-),故B正确;
C.硫化钠溶液中,钠离子不水解,硫离子水解生成硫氢根离子,硫离子和硫氢根离子水解都生成氢氧根离子,所以c(OH-)>c(HS-),但硫离子和硫氢根离子水解都较微弱,所以离子浓度大小顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-),故C正确;
D.根据质子守恒得c(OH-)=c(HS-)+c(H+)+2c(H2S),故D错误;
故选D.
点评 本题考查了电解质溶液中电荷守恒、物料守恒、离子浓度大小比较等知识点,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的邻位二元取代物只有一种 | B. | 苯的间位二元取代物只有一种 | ||
| C. | 苯的对位二元取代物只有一种 | D. | 苯的邻位二元取代物有二种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的颜色不再改变 | B. | 混合气体的密度不再改变 | ||
| C. | 混合气体的压强不再改变 | D. | 混合气体的平均分子质量不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间t(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
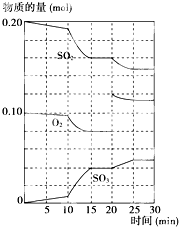 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)(△H<0)
在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g)?2SO3(g)(△H<0)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
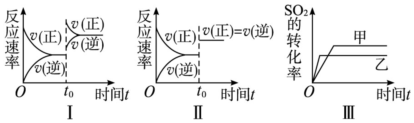
| A. | 图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 | |
| B. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较低 | |
| C. | 图Ⅲ研究的是催化剂对平衡的影响,且甲的催化效率比乙高 | |
| D. | 图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com