
火法炼铜得到的粗铜中含多种杂质(如锌、金和银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯.在电解精炼时()
A. 粗铜接电源负极
B. 纯铜作阳极
C. 杂质都将以单质形式沉积到池底
D. 纯铜片增重2.56g,电路中通过电子为0.08mol
考点: 原电池和电解池的工作原理.
专题: 电化学专题.
分析: A、电解精炼铜,粗铜作阳极,与电源正极相连;
B、电解精炼铜,粗铜作阳极,精铜作阴极;
C、不如铜活泼的金属不参与阳极反应,比铜活泼的金属参与阳极反应,不参与阳极放电的金属单质以及杂质会形成阳极泥;
D、精铜片增重2.56g,即析出2.56g铜,则电路中通过电子为 ×2=0.08mol.
×2=0.08mol.
解答: 解:A、电解精炼铜,粗铜作阳极,粗铜作阳极,与电源正极相连,故A错误;
B、电解精炼铜,粗铜作阳极,精铜作阴极,故B错误;
C、在阳极上,不参与放电的金属单质金、银等贵重金属以及杂质会形成阳极泥沉积到池底,故C错误;
D、精铜片增重2.56g,即析出2.56g铜,则电路中通过电子为 ×2=0.08mol,故D正确;
×2=0.08mol,故D正确;
故选D.
点评: 本题考查学生电解精炼铜的原理,注意电解池的工作原理是关键,难度不大.


科目:高中化学 来源: 题型:
关于溶液的酸碱性说法正确的是()
A. c(H+)很小的溶液一定呈碱性
B. PH=7的溶液一定呈中性
C. c(OH﹣)=c(H+)的溶液一定呈中性
D. 不能使酚酞试液变红的溶液一定呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质);
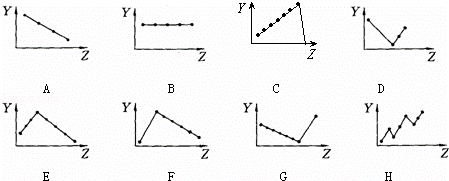
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数 (2)ⅦA族元素氢化物的沸点
(3)第三周期元素单质的熔点 (4)第三周期元素的最高正化合价
(5)IA族元素单质熔点 (6)F﹣、Na+、Mg2+、Al3+四种离子的离子半径 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H1=﹣Q1,H2(g)+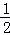 O2(g)═H2O(g);△H2=﹣Q2,H2(g)+
O2(g)═H2O(g);△H2=﹣Q2,H2(g)+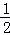 O2(g)═H2O(l);△H3=﹣Q3,常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况)经完全燃烧恢复到常温,放出的热量为()
O2(g)═H2O(l);△H3=﹣Q3,常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(已折合成标准状况)经完全燃烧恢复到常温,放出的热量为()
A. 0.4Q1+0.05Q2 B. 0.4Q1+0.1Q2 C. 0.4Q1+0.05Q3 D. 0.4Q1+0.1Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量).
(1)反应的热化学方程式为 .
(2)又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ.
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极分别电解下列各物质的水溶液,一段时间后,向剩余电解质溶液中加入适量相应的溶质能使溶液恢复到电解前浓度的是()
A. AgNO3 B. Na2SO4 C. CuCl2 D. KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解物质的量浓度相同、体积比为1:3的CuSO4和NaCl的混合溶液,可能发生的反应有()
①2Cu2++2H2O 2Cu+4H++O2↑
2Cu+4H++O2↑
②Cu2++2Cl﹣ Cu+Cl2↑
Cu+Cl2↑
③2Cl﹣+2H2O 2OH﹣+H2↑+Cl2↑
2OH﹣+H2↑+Cl2↑
④2H2O 2H2↑+O2↑
2H2↑+O2↑
A. ①②③ B. ①②④ C. ②③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是
A.明矾常作净水剂
B.与铜质水龙头连接处的钢质水管易发生腐蚀
C.在水果贮藏室中,放几块被KMnO4溶液浸透过的“砖块”,可延长水果保存时间
D.汽车尾气中的CO、NO等都是汽油和柴油的不完全燃烧产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com