
下列生产或实验事实引出的相应结论不正确的是 ( )
| 选项 | 事实 | 结论 |
| A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| B | 工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使SO3的吸收速率增大 |
| C | 在容积可变的密闭容器中发生反应:2NH3(g) | 正反应速率加快,逆反应速率减慢 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
向某恒容密闭容器中充入一定量CO2和H2,发生反应:CO2(g)+ H2(g)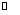 HCOOH(g),测得平衡体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
HCOOH(g),测得平衡体系中CO2的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
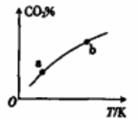
A. 正反应速率
B. 逆反应速率
C. HCOOH(g)的浓度
D. H2的体积分数
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中错误的是( )
A. 盐类都能水解
B. 配制FeCl3溶液,为了抑制水解,常加入盐酸
C. 盐类的水解反应,通常是吸热反应
D. 盐类水解是指组成盐的离子跟水电离出来的H+或OH—生成弱电解质的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g)===4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加
了0.45 mol,则此反应的速率v(X)(反应物的消耗速率或产物的生成速率)可表示为( )
A.v(NH3)=0.010 mol·L-1·s-1 B.v(O2)=0.001 0 mol·L-1·s-1
C.v(NO)=0.001 0 mol·L-1·s-1 D.v(H2O)=0.045 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的A和B混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g),经5 分
钟后,测得 D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol·L-1·min-1。A在5
D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,C的平均反应速率是0.1 mol·L-1·min-1。A在5
min末的浓度是________,B的平均反应速率是________,D的平均反应速率是________,x的值是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度
为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K ,每次实
,每次实
验HNO3的用量为25.0 mL,大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol·L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3的浓度对该反应速率的影响; (Ⅱ)实验①和________探究温度对该反应速率的影响; (Ⅲ)实验①和________探究大理石规格 (粗、细)对该反应速率的影响。 |
| ② | ||||
| ③ | ||||
| ④ |
(2)实验①中CO2质量随时间变化的关系见下图:
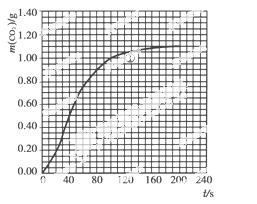
依据反应方程式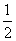 CaCO3+HNO3===
CaCO3+HNO3===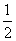 Ca(NO3)2+
Ca(NO3)2+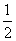 CO2↑+
CO2↑+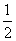 H2O,计算实验①在70~90 s范围内HNO3的反应速率(忽略溶液体积变化,写出计算过程)。
H2O,计算实验①在70~90 s范围内HNO3的反应速率(忽略溶液体积变化,写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如下图所示。下列判断正确的是
A.在0~50 min之间,pH=2和pH=7时R的降解
百分率相等
B.溶液酸性越强,R的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在20~25 min之间, pH=10时R的平均降解速率为
0.04 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
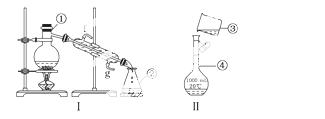
(1)写出下列仪器的名称:
① ,② ,④ 。
(2)仪器①~④中,使用时必须检查是否漏水的有 (填序号)。
(3)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有 ,将仪器补充完整后进行的实验操作的名称为 ;冷凝管的进水口是 (填“f”或“g”);现需配制250 mL 0.2 mol/L NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,图中的错误是:  。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)取少量Fe2O3粉末(红棕色)加入适量盐酸,反应的离子方程式为 。
反应后得到棕黄色的FeCl3溶液.用此溶液做以下实验:
(2)取少量溶液置于试管中,滴入NaOH溶液,看到有红褐色沉淀生成,反应的离子方程式为 .
(3)在小烧杯中加入25 mL蒸馏水,加热至沸腾后,向沸水中加入2 mL FeCl3饱和溶液,继续煮沸至溶液呈 色,即可制得Fe(OH)3胶体.
(4)另取一小烧杯也加入25 mL蒸馏水后,向烧杯中也加入2 mL FeCl3饱和溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的 烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到 烧杯中会产生丁达尔效应.此实验可以区别 .
烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到 烧杯中会产生丁达尔效应.此实验可以区别 .
(5)取乙烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加一定量的稀盐酸,边滴边振荡,可以看到的现象是 ,
此变化的离子 方程式为 。
方程式为 。
(6)已知明矾能净水,理由是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com