
在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是()
A. 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B. 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
C. 向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
D. 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl﹣
考点: 氯气的化学性质.
专题: 卤族元素.
分析: 溶液中存在平衡Cl2+H2O⇌HCl+HClO,只有氯气有颜色,为黄绿色,氯水中含有氯气而呈浅黄绿色,溶液中HCl与硝酸银反应产生AgCl白色沉淀,而溶液呈酸性,能与碳酸氢钠反应生成二氧化碳,溶液中氯气、HClO都强氧化性,都可以将亚铁离子氧化为铁离子,而使溶液变为棕黄色.
解答: 解:溶液中存在平衡Cl2+H2O⇌HCl+HClO,
A.只有氯气有颜色,为黄绿色,氯水呈浅黄绿色是由于含有氯气,故A正确;
B.溶液呈酸性,能与碳酸氢钠反应生成二氧化碳,故B正确;
C.溶液中氯气、HClO都强氧化性,都可以将亚铁离子氧化为铁离子,而使溶液变为棕黄色,不能说明氯水中含有HClO,故C错误;
D.溶液与硝酸银反应产生白色沉淀,只能是氯离子与银离子反应得到AgCl白色沉淀,说明氯水中含有Cl﹣,故D正确;
故选C.
点评: 本题考查氯水的性质,难度不大,侧重对基础知识的考查,需要学生熟练掌握基础知识.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
设以为阿伏伽德罗常数的值,下列叙述中正确的是( )
A. 92 g NO2和N204混合气体中含有的原子数为3NA
B. 标准状况下,11.2 L H2O中含有的电子数为20NA
C. 0.5mol•L“的Ba(0H)2溶液中0H一的数目为NA
D. 1 mol Mg与足量的02或N2反应生成MgO或Mg3N2时,失去的电子数均为2N
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g),在10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率V(x)可表示为()
A. V(NH3)=0.0010mol•L﹣1•S﹣1 B. V(O2)=0.0010 mol•L﹣1•S﹣1
C. V(NO)=0.010 mol•L﹣1•S﹣1 D. V(H2O)=0.045 mol•L﹣1•S﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是()
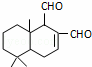
A. Br2的CCl4溶液 B. Ag(NH3)2OH溶液
C. HBr D. H2
查看答案和解析>>
科目:高中化学 来源: 题型:
雾霾会影响人们的生活与健康.某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42﹣、NO3﹣、Cl﹣.某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下的实验:
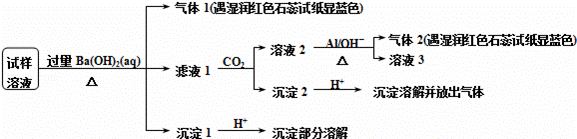
已知:3NO3﹣+8Al+5OH﹣+2H2O 3NH3↑+8AlO2﹣
3NH3↑+8AlO2﹣
根据以上的实验操作与现象,该同学得出的结论错误的是()
A. 试样中肯定存在NH4+、Mg2+、SO42﹣和NO3﹣
B. 试样中可能存在Na+、Cl﹣
C. 试样中一定不含Al3+
D. 可以确定该雾霾的成分是NaNO3、NH4Cl和MgSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A有稳定性好、抗氧化能力强的特点,其结构如图 .分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(
.分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(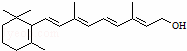 )和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
)和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
完成下列填空:
(1)化合物B能发生下列哪种类型的反应
a.取代反应b.加成反应c.缩聚反应d.氧化反应
(2)化合物C能经下列反应得到G(分子式为C8H6O2,分子内含五元环).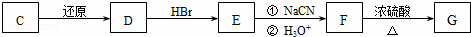
已知:ROOH RCH2OH RX
RCH2OH RX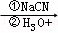 RCOOH
RCOOH
化合物C的结构简式为 .
(3)反应F→G的化学方程式为
(4)化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环上有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式、、.
查看答案和解析>>
科目:高中化学 来源: 题型:
利用“化学蒸气转移法”制备TaS2晶体,某温度下的2L恒容密闭容器中加入一定量 的 I2(g)和TaS2(s)发生如下反应:TaS2(s)+2I2(g)⇌TaI4(g)+S2(g)△H=a kJ•mol﹣1 (Ⅰ)达平衡时,TaS2(s)、I2(g)、TaI4(g)、S2(g)的物质的量分别为3mol、2mol、2mol、2mol.
(1)反应(Ⅰ)的平衡常数表达式K=
(2)若该温度下该容器中某时刻TaS2(s)、I2(g)、TaI4(g)、S2(g)的物质的量分别为2mol、2mol、4mol、4mol,则该时刻平衡向 (填“正反应”或“逆反应”)移动,v正 v逆(填“>”、“=”或“<”).
(3)在不同温度下,该反应的平衡常数K如下表:
| 温度/℃ | 40 | 80 | 200 |
| 平衡常数K | 1 | 1.5 | 4 |
该反应的△H 0(填“>”、“=”或“<”).
(4)40℃时,向该恒容密闭容器中加入2mol I2(g)和4mol TaS2(s),I2(g)的平衡转化率为 写出计算过程,结果保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子的检验方法中正确的是( )
|
| A. | 某溶液加AgNO3溶液生成白色沉淀,说明原溶液中有Cl﹣ |
|
| B. | 某溶液加BaCl2溶液生成白色沉淀,说明原溶液中有SO42﹣ |
|
| C. | 某溶液加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+ |
|
| D. | 某溶液加KOH溶液生成红褐色沉淀,说明原溶液中有Mg2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com