
 CH3OH(g)+H2O(g) +49.0 kJ����Ӧ��2����ʱ�ﵽ��ƽ�⡣
CH3OH(g)+H2O(g) +49.0 kJ����Ӧ��2����ʱ�ﵽ��ƽ�⡣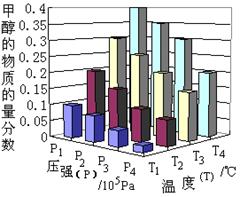
| A��P3��P2T3��T2 | B��P2��P4T4��T2 |
| C��P1��P3T1��T3 | D��P1��P4T2��T3 |
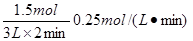


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 N2O4����ɫ������H<0������Ӧ��NO2��N2O4�����ʵ����淴Ӧʱ��仯����������ͼ��������Ҫ������
N2O4����ɫ������H<0������Ӧ��NO2��N2O4�����ʵ����淴Ӧʱ��仯����������ͼ��������Ҫ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3������˵���ܱ����÷�Ӧ�ﵽƽ��״̬���ǣ� ��
2NH3������˵���ܱ����÷�Ӧ�ﵽƽ��״̬���ǣ� ��| A�����ɰ���������ֽⰱ��������� |
| B���Ͽ�һ��N��N��ͬʱ������N-H������ |
| C��N2��H2����NH3��Ũ����� |
| D�����������ѹ���ٸı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ˮƿʱ���д���������� |
B����2HI(g)  H2(g) + I2(g)������ƽ����ϵѹǿ��ʹ��ɫ���� H2(g) + I2(g)������ƽ����ϵѹǿ��ʹ��ɫ���� |
| C���ںϳɰ��ķ�Ӧ�У�Ϊ���NH3�IJ��ʣ���ȡ��ѹ������ |
D����ˮ����Br2 + H2O HBr + HBrO��������AgNO3��Һ����Һ��ɫ��dz HBr + HBrO��������AgNO3��Һ����Һ��ɫ��dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
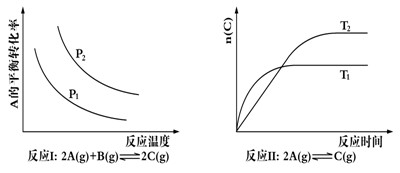
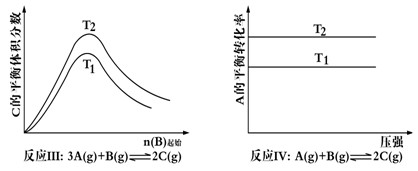
| A����Ӧ���H> 0��P2>P1 | B����Ӧ���H<0��T1>T2 |
| C����Ӧ���H> 0,T2>T1;���H<0,T2<T1 | D����Ӧ����H<0��T2>T1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2HI(g)������һ������ƽ��״̬����
2HI(g)������һ������ƽ��״̬����| A�����������ɫ���ٸı�ʱ |
| B���������������ʵ��ڵ⻯�����������ʱ |
| C��������Ũ�ȵ��ڵ�������Ũ��ʱ |
| D����������ƽ����Է�����������ʱ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
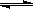 Y+Z,�仯ѧ��Ӧ������ʱ��仯��ͼ����ͼ��ʾ������t1ʱ�̴ﵽƽ�⣬t2ʱ����С���������t3ʱ�����´ﵽƽ�⣬�����й�˵������ȷ����( )
Y+Z,�仯ѧ��Ӧ������ʱ��仯��ͼ����ͼ��ʾ������t1ʱ�̴ﵽƽ�⣬t2ʱ����С���������t3ʱ�����´ﵽƽ�⣬�����й�˵������ȷ����( )
| A��X�ڸ�������һ����Ϊ���� |
| B��Y��Z�ڸ�������������һ��Ϊ���� |
| C��t1ʱ�̴ﵽƽ��ʱ��t3ʱ��ƽ��ʱ����̬���ʵ�Ũ����ͬ |
| D����t1��t3��ƽ�Ⲣδ�����ƶ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3Z(g)������Ӧ��ʼʱ����2mol X��2mol Y����ƽ���Y���������Ϊa%��������������ʱ�������������������Ϊ��ʼ���ʣ�ƽ���Y�����������a%����
3Z(g)������Ӧ��ʼʱ����2mol X��2mol Y����ƽ���Y���������Ϊa%��������������ʱ�������������������Ϊ��ʼ���ʣ�ƽ���Y�����������a%����| A��1molY��1molZ | B��2mol X��1molY��1molZ | C��1molY��3molZ | D��2molZ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
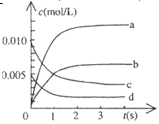
 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010. | 0.008 | 0.007 | 0. 007 | 0.007 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com