
【题目】一定量的氢气在氯气中燃烧,所得混合物用100mL质量分数为20%,密度为1.2g/cm3的NaOH溶液吸收,恰好完全吸收,测得溶液中含有NaClO的物质的量为0.1mol。
(1)原NaOH溶液的物质的量浓度为___mol/L;
(2)所得溶液中Cl-的物质的量为___mol;
(3)原混合气体中氯气和氢气的物质的量之比为___。
【答案】6 0.5 3:2
【解析】
先将氢氧化钠物质的量浓度计算出来,再求出物质的量,在 根据钠元素守恒求出氯离子物质的量,在根据比例关系求氢气与氯气的比。
⑴![]()
故答案为6;
⑵NaOH最终生成氯化钠和次氯酸钠,根据钠元素守恒
n(Cl-)=n(NaCl)=6 molL-1×0.1L – 0.1 mol = 0.5 mol
故答案为0.5
⑶根据2NaOH + Cl2 === NaClO +NaCl + H2O,生成0.1 mol NaClO,反应消耗0.1mol Cl2,也生成0.1 mol NaCl,因此HCl与氢氧化钠反应生成0.4 molNaCl,即有0.4molHCl生成,则消耗氢气和氯气分别为0.2mol,总的消耗氯气为0.3 mol,故原混合气体中氯气和氢气的物质的量之比为3:2,
故答案为3:2.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
【题目】(1)标准状况下,与5.6L的CH4气体含相同H原子数的硫化氢的质量为___g。
(2)将2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=__mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g/cm3的浓硫酸,配制480mL浓度成0.2mol·L-1 稀硫酸,计算需要量取____mL的浓硫酸。
(3)配平以下方程式___
___K2Cr2O7+___HCl=___KCl+___CrCl3+___Cl2↑+___H2O
上述反应中物质氧化性:___>__,每生成lmolCl2时有__个电子发生转移,氧化剂与还原剂的物质的量之比为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中一定大量共存的是( )
A. 含有AlO2-的溶液中:Na+ 、Al3+、Cl-、K+
B. 常温下由水电离出的c(H+)·c(OH-)=10-20 mol2·L-2的溶液中:Na+、NH![]() 、Cl-
、Cl-
C. 常温下 c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
D. 在c(H+)=1.0×10-13 mol·L-1的溶液中:Na+、S2-、AlO2-、SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将大烧杯丙扣在甲乙两个小烧杯(口向上)上。向两个小烧杯中分别装入如下表所列的试剂进行实验。实验现象与预测现象不同的是
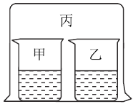
甲中试剂 | 乙中试剂 | 预测现象 | |
A | 浓盐酸 | 硝酸银溶液 | 乙中产生白色沉淀 |
B | 浓氨水 | 硫酸铁溶液 | 乙中产生红褐色沉淀 |
C | 浓盐酸 | 浓氨水 | 丙中产生白色烟雾 |
D | 氯化铝溶液 | 浓氨水并加入 固体氢氧化钠 | 甲中先产生白色沉淀,后又沉淀消失 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.200 0 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是______(填编号)。若测定结果偏高,其原因可能是________(填字母)。
A.配制标准溶液的固体NaOH中混有KOH杂质
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.所配的标准NaOH溶液物质的量浓度偏大
(2)判断滴定终点的现象是_____________________________________。
(3)如图是某次滴定时的滴定管中的液面,其读数为________mL。
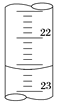
(4)根据下列数据,请计算待测盐酸的浓度:________mol·L-1。
滴定次数 | 待测体积(mL) | 标准烧碱溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 2.00 | 24.10 |
第三次 | 20.00 | 4.00 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A. 使体积不变,增加H2O的量 B. 将容器的体积缩小一半
C. 使体积不变,充氦气使体系压强增大 D. 使压强不变,充氦气使容器体积增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯霉素(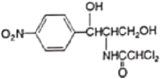 )曾用作广谱抗菌药物,一种合成路线如下:
)曾用作广谱抗菌药物,一种合成路线如下:
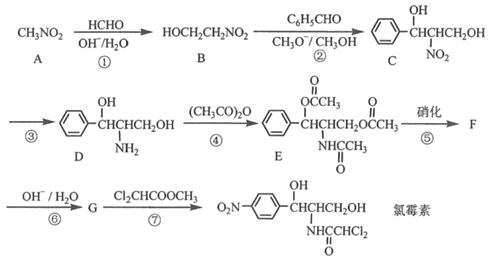
已知: 的性质与酯基相似。
的性质与酯基相似。
(1)A的化学名称为___________。
(2)D所含官能团的名称为___________;可以检测有机化合物中存在何种官能团的仪器是__________。
(3)反应②和③的反应类型分别是___________、_____________。
(4)设计反应④和⑥的目的是_________________________________________。
(5)由F到G的化学方程式为_________________________________________。
(6)芳香化合物X(C6H7NO2),与D具有相同的官能团,X的可能结构共有________种(不考虑立体异构):其中核磁共振氢谱为四组峰,峰面积比为2:2:2:1,其结构简式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是(____)
A.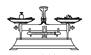 称量
称量
B.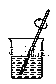 溶解
溶解
C.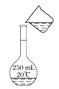 转移溶液
转移溶液
D.![]() 定容
定容
(2)下列几种导电性变化图像,把符合要求的图像序号填在相应的题目后面括号中。
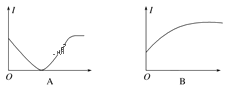
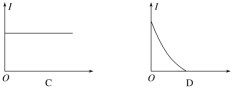
①向H2SO4溶液中加入等体积、等物质的量浓度的Ba(OH)2溶液(____)
②向AgNO3溶液通入少量HCl(____)
③向氨水中通入HCl直至过量(____)
④向饱和石灰水中不断通入CO2(____)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com