
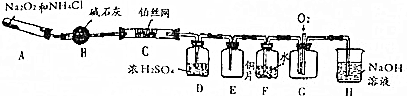
���� ��1��A�з�����Ӧ���Ȼ�立ֽ����ɰ������Ȼ��⣬�Ȼ�����������Ʒ�Ӧ�����Ȼ��ƺ�ˮ��������
��2��Ũ����������Ժ���ˮ�ԣ���������NO��NH3��NO�ᱻO2��������NO2�����ڿ����е�ˮ������Ӧ����HNO3����HNO3��NH3��������̣�
��3��ͭ��ϡ���ᷴӦ��������ͭ��һ��������ˮ����������������Ի����¾���ǿ�������ԣ��ܹ��ܽ�ͭ��
��4���ɷ���ʽ2NO2+2NaOH=NaNO2+NaNO3+H2O��NO+NO2+2NaOH=2NaNO2+H2O��֪��NO�������ܱ����գ�NO��NO2������屻NaOH��Һ����ȫ���գ�����n��NO2����n��NO����1����n��NO2����n��NO��=1ʱxֵ��С������x����Сֵ����Ϊ����NO������x���ֵ��2���ݴ�ȷ��xȡֵ��Χ��
��� �⣺��1��A�з�����Ӧ���Ȼ�立ֽ����ɰ������Ȼ��⣬�Ȼ�����������Ʒ�Ӧ�����Ȼ��ƺ�ˮ������������ʽ��NH4Cl$\frac{\underline{\;����\;}}{\;}$NH3��+HCl����2Na2O2+4HCl=4NaCl+O2��+2H2O��
�ʴ�Ϊ��NH4Cl$\frac{\underline{\;����\;}}{\;}$NH3��+HCl����2Na2O2+4HCl=4NaCl+O2��2H2O+��
��2��Ũ����������Ժ���ˮ�ԣ�����װ��D���ó�ȥ������ˮ������
��������NO��NH3��NO�ᱻO2��������NO2�����ڿ����е�ˮ������Ӧ����HNO3����HNO3��NH3��������̣�
��ȡ��D��һ��������������Ӧ���ɵĶ���������ˮ��Ӧ�������ᣬ����Ͱ�����Ӧ��������粒��壬������E�н��۲쵽�������̣�
�ʴ�Ϊ����ȥ������ˮ���������ɵ�NO��O2��Ӧ����NO2��NO2��ˮ��Ӧ����HNO3��NH3��HNO3��Ӧ����NH4NO3��
��3��ͭ��ϡ���ᷴӦ��������ͭ��һ��������ˮ�����ӷ���ʽ��2NO3-+3Cu+8H+�T3Cu2++2NO��+4H2O��
��������������Ի����¾���ǿ�������ԣ��ܹ��ܽ�ͭ��Ϊ��ʹͭƬ���ܽ����ʼӿ죬����װ��F�м������������������BC��
�ʴ�Ϊ��2NO3-+3Cu+8H+�T3Cu2++2NO��+4H2O��BC��
��4���ɷ���ʽ��֪��NO�������ܱ����գ�NO��NO2������屻NaOH��Һ����ȫ���գ�����n��NO2����n��NO����1����n��NO2����n��NO��=1ʱxֵ��С��x��СֵΪ��$\frac{2+1}{2}$=1.5����Ϊ����NO������x���ֵ��2����x��ȡֵ��ΧΪ1.5��x��2��
�ʴ�Ϊ��1.5��x��2��
���� ���⿼���˰�����������Ʊ������ʼ��飬��ȷ����������������ǽ���ؼ���ע����������������Ի����µ�ǿ�����ԣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO3 | B�� | N2O5 | C�� | Na2O | D�� | CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ư��Һ��ͨ������CO2��2ClO-+CO2+H2O�T2HClO+CO32- | |
| B�� | �ð�ˮ����������������SO2+NH3•H2O�THSO3-+NH4+ | |
| C�� | ������������������Һ���ն���������3NO2+2OH-�T2NO3-+NO+H2O | |
| D�� | ���������Һ��ͨ������SO2���壺Ca2++2ClO-+SO2+H2O�TCaSO3��+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʷе㣺W��Y | |
| B�� | X������������Ӧ��ˮ��������Y�������ﷴӦ | |
| C�� | W��X�γɵĻ������к��й��ۼ� | |
| D�� | �����ӵİ뾶��X��Y��Z |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�11.2LCHCl3���й��ۼ���Ϊ2NA | |
| B�� | ij�¶��£���ˮpH=6�����¶���1LpH=11��NaOH��Һ�к���OH-��ĿΪ0.1NA | |
| C�� | ��3.65gHCl��ˮ��Һ�к���������Ϊ0.2NA | |
| D�� | 0.2mol/LNa2S��Һ�к���S2-��ĿС��0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
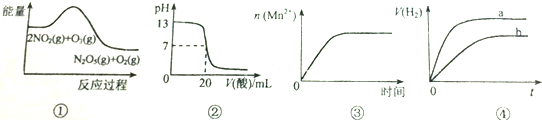
| A�� | �ٱ�ʾ��ѧ��Ӧ2NO2��g��+O3��g���TN2O5��g��+O2��g����H��0 | |
| B�� | �ڱ�ʾ25��ʱ����0.5mol/LCH3COOH��Һ�ζ�20mlNaOH��Һ����Һ��pH�����������ı仯 | |
| C�� | �۱�ʾ10ml 0.01mol/L KMnO4 ������Һ�������0.1mol/L H2C2O4��Һ���ʱ��n��Mn2+�� ��ʱ��ı仯 | |
| D�� | �ܱ�ʾ�����pH����ͬ��HCl��CH3COOH������Һ�У��ֱ����������п������H2�������ʱ��ı仯����a��ʾCH3COOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �κ��������кͷ�Ӧ����1mol H2O�Ĺ����У������仯����ͬ | |
| B�� | ��֪��C ��s��ʯī��=C ��s�����ʯ����H=+1.5 kJ•mol-1������ʯ��ʯī���ȶ� | |
| C�� | ����2H2 ��g��+O2 ��g��=2H2O ��g����H=-a kJ•mol-1����2H2 ��g��+O2 ��g��=2H2O ��l����H=-b kJ•mol-1���� b��a | |
| D�� | ���Է����еķ�Ӧһ���Ƿ��ȷ�Ӧ�������Է����еķ�Ӧһ�������ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ζ��ܡ���Һ���Լ��ζ�����������ʢ����Һ����ƿ��ʹ��ǰ����Ҫϴ������ϴ | |
| B�� | ʵ������ȡ����ʱ����װ�ö������̣��ټ��װ�õ������� | |
| C�� | �����ɫש�����Ƿ��������IJ���Ϊ����Ʒ���������ˮ�ܽ�����ˡ�����Һ�еμ�KSCN��Һ | |
| D�� | ���к��Ȳⶨ��ʵ���У�������������Һ�������Ϸ�Ӧ�������¶���Ϊĩ�¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
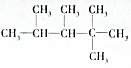 �����������ϩ�����ܵĽṹ��ʽ��CH2=CHCH3CHCH3C��CH3��3����CH3��2C=CCH3C��CH3��3����CH3��2CHC=CH2C��CH3��3��
�����������ϩ�����ܵĽṹ��ʽ��CH2=CHCH3CHCH3C��CH3��3����CH3��2C=CCH3C��CH3��3����CH3��2CHC=CH2C��CH3��3��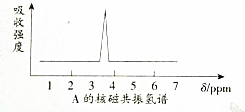
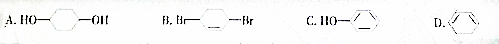
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com