
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
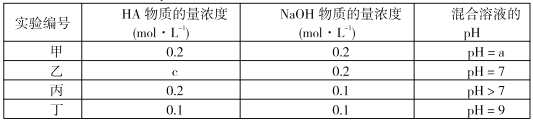
(1)不考虑其它组的实验结果,单从甲组情况分析.如何用a(混合溶液的pH)来说明HA是强酸还是弱酸____________________。
(2)不考虑其它组的实验结果.单从乙组情况分析,C是否一定等于0.2_________(选填“是”或“否”)。混合液中离子浓度c(A-)与c(Na+)的大小关系是___________。
(3)丙组实验结果分析,HA是___________酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是_______________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=__________mol/L。
【答案】
(1)若a=7,则HA是强酸;若a>7,则HA是弱酸;
(2)否;c(A-)=c(Na+)
(3)弱;c(Na+)>c(A-)>c(OH-)>c(H+)
(4)10-5
【解析】
试题分析:(1)不考虑其它组的实验结果,单从甲组情况分析,若a=7,则HA是强酸;若a>7,则HA是弱酸,故答案为:若a=7,则HA是强酸;若a>7,则HA是弱酸;
(2)不考虑其它组的实验结果,单从乙组情况分析,pH=7,若HA为强酸,则C等于0.2,若HA为弱酸,则C大于0.2,所以C不一定为0.2,溶液中存在电荷守恒:c(Na+)+c(H+)=c(A-)+c(OH-),因pH=7,则c(OH-)=c(H+),则c(A-)=c(Na+),故答案为:否;c(A-)=c(Na+);
(3)HA物质的量浓度为0.2mol/L,而NaOH物质的量浓度为0.1mol/L,pH>7,所以HA是弱酸,丙组得到的溶液为0.05mol/L的HA和0.05mol/L的NaH的混合液,根据电荷守恒可以得到c(OH-)+c(A-)=c(Na+)+c(H+),由于pH>7,所以c(OH-)>c(H+),即c(Na+)>c(A-),所以混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+),故答案为:弱;c(Na+)>c(A-)>c(OH-)>c(H+);
(4)丁组实验所得混合溶液为浓度为0.05mol/L的NaA溶液,其pH为9,促进水的电离,OH-全部为水电离,所以由水电离出的c(OH-)=10-5mol/L,故答案为:10-5。


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】科学家开发出一种新型锂-氧电池,其能世密度极高,效率达到90%以上,电池中添加碘化锂(LiI)和微量水。工作原理如图所示,总反应为:O2+4LiI+2H2Og![]() 2I2+4LiOH。对于该电池的下列说法不正确的是
2I2+4LiOH。对于该电池的下列说法不正确的是

A.充电时阴极反应为LiOH+e-=Li+OH-
B.充电时Li+从阳极区移向阴极区
C.放电时正极反应为O2+2H2O+4Li++4e-=4LiOH
D.放电时负极上I-被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A. 两种元素组成的分子中一定只有极性键
B. 非金属元素组成的化合物一定是共价化合物
C. 干冰升华时,分子内共价键会发生断裂
D. 含有阴离子的化合物中一定含有阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中能大量共存,溶液呈现无色,且加入一小块钠后仍然能大量共存的是( )
A.K+、MnO4-、SO42-、H+
B.Ba2+、Na+、HCO3-、NO3-
C.Na+、NO3-、K+、Cl-
D.Ca2+、NO3-、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是
A.植物油不能使溴的四氯化碳溶液褪色
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后(假设混合液体积为二者之和),所得溶液中部分微粒组分及浓度如图所示,下列说法不正确的是
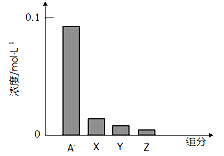
A.HA是弱酸
B.该混合液pH > 7
C.该混合溶液中:c(A-)+c(Y)=c(Na+)
D.图中x表示HA,Y表示OH-,Z表示H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.普通锌锰干电池中的MnO2在工作时起催化作用
B.lmol Na2O2与足量水反应产生O2,理论上转移的电子数约为2×6.02×1023
C.室温下,体积、pH均相同的HA和HB两种一元酸分别与足量的锌反应,HA放出氢气多,说明酸性:HB>HA
D.恒温恒压密闭容器中反应N2(g)+3H2(g)![]() 2NH3(g)ΔH=-a kJ·mol-1达到平衡时,向容器中再充入一定量NH3, 重新达平衡时a值减小
2NH3(g)ΔH=-a kJ·mol-1达到平衡时,向容器中再充入一定量NH3, 重新达平衡时a值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铅蓄电池电解AgNO3、Na2SO3的溶液,a、b、c、d电极材料均为石墨,已知铅蓄电池的总反应为:Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(1)通电时a电极质量增加,下列说法正确的是
2PbSO4(s)+2H2O(1)通电时a电极质量增加,下列说法正确的是
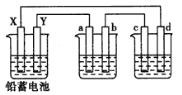
A.电路中通过1mol电子时,Y电极质量增加48g
B.放电时铅蓄电池负极的电极反应式为:PbO2(s)+4H+(aq)+SO42-(aq)+2e-===PbSO4(s)+2H2O(l)
C.c、d电极产生气体的物质的量之比为1∶2
D.X极为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工厂常用浓氨水检验管道是否漏氯气,反应的化学方程式为:3Cl2+8NH3=6NH4Cl+N2,当有10.65gCl2消耗时,被氧化的氨的质量为( )
A.3.4g B.1.7g C.6.8g D.0.85g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com