
 BCl3����Ҫ�Ļ���ԭ�ϣ���е�12�森500��ʱ����2L���ܱ������а�һ������Ͷ��B2O3��C��Cl2��ģ�ҵ��ȡ���Ȼ���ķ�Ӧ���£�B2O3��s��+3C��s��+3Cl2��g��?2BCl3 ��g��+3CO��g����
BCl3����Ҫ�Ļ���ԭ�ϣ���е�12�森500��ʱ����2L���ܱ������а�һ������Ͷ��B2O3��C��Cl2��ģ�ҵ��ȡ���Ȼ���ķ�Ӧ���£�B2O3��s��+3C��s��+3Cl2��g��?2BCl3 ��g��+3CO��g�������� ��1�����ݹ���������仯������ʵ����仯����������������ʵ���������ƽ����Ӧ����v=$\frac{��c}{��t}$�����㣻
��2��A����ѧƽ��Ľ����Ǵ������ҽ����ģ�
B�����ŷ�Ӧ�Ľ��У���Ӧ����������
C����Ӧ��ʼ��ƽ�⣬����������ܶȦ�=$\frac{m}{V}$���жϣ�
D�������ڵ�ѹǿ���ٱ仯��֤���ﵽ��ƽ�⣻
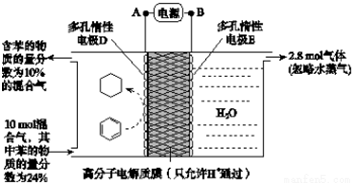
��3���ٸ���ͼ֪�����е�̼�õ������ɻ����飬��D��������E������������A�Ǹ�����B�����������ӴӸ�������������
�ڸ�ʵ���Ŀ���Ǵ��⣬���������Ϸ����ķ�ӦΪ����Ŀ���������ϱ��õ��Ӻ����������ɻ����飻
������������������ͬʱ���������ӣ������ϱ��õ��Ӻ������ӷ�Ӧ���ɻ����飬���μӷ�Ӧ��Ҫ���ӵ����ʵ�������ת�Ƶ��ӵ����ʵ���֮�Ⱦ��ǵ���Ч�ʦǣ�
��� �⣺��1�����������ʵ����仯$\frac{15.84g��3}{106g/mol}$=0.448mol����ƽ����Ӧ����v=$\frac{��c}{��t}$=$\frac{0.448mol}{2L��3min}$=0.075 mol/��L•min����
�ʴ�Ϊ��0.075 mol/��L•min����
��2��A����ѧƽ��Ľ����Ǵ������ҽ����ģ�����Ӧ���ʽϴ�����3minʱ��CO����������С���������������ʣ���A����
B�����ŷ�Ӧ�Ľ��У���Ӧ����������2min��4minʱBCl3���������ʱ�0��2minʱ��������B����
C����Ӧ��ʼ��ƽ�⣬������ܶȦ�=$\frac{m}{V}$������������������ģ�V���䣬�����ܶ�������C��ȷ��
D���÷�Ӧ��һ��ǰ������ϵ���Ͳ���ȵķ�Ӧ�������ڵ�ѹǿ���ٱ仯����֤���ﵽ��ƽ�⣬��D��ȷ��
�ʴ�Ϊ��CD��
��3���ٸ���ͼ֪�����е�̼�õ������ɻ����飬��D��������E������������A�Ǹ�����B�����������ӴӸ����������������Ե��Ӵ�A����D���ʴ�Ϊ��A��D��
�ڸ�ʵ���Ŀ���Ǵ��⣬���������Ϸ����ķ�ӦΪ����Ŀ���������ϱ��õ��Ӻ����������ɻ����飬�缫��ӦʽΪC6H6+6H++6e-=C6H12��
�ʴ�Ϊ��C6H6+6H++6e-=C6H12��
�����������������ӷŵ���������������������2.8mol������ת�Ƶ��ӵ����ʵ���=2.8mol��4=11.2mol������1mol����ʱ����2mol������������2.8mol����ʱͬʱ����5.6mol��������μӷ�Ӧ�ı������ʵ�����xmol���μӷ�Ӧ�����������ʵ�����3xmol��ʣ�౽�����ʵ���Ϊ10mol��24%-xmol����Ӧ�ĺ���$\frac{10mol��24%-x}{10mol-3xmol+5.6mol}$��100%=10%��x=1.2����ת��Ϊ������ת�Ƶ��ӵ����ʵ���Ϊ1.2mol��6=7.2mol���� $\frac{7.2mol}{11.2mol}$��100%=64.3%��
�ʴ�Ϊ��64.3%��
���� ���⿼���˻�ѧ��Ӧ���ʵļ��㡢��ѧƽ���ƶ������ԭ����Ӧ�õ�֪ʶ�������ۺ�֪ʶ�Ŀ��飬��Ŀ�Ѷ��еȣ�ע��������ʹ�ʽ��Ӧ�ú͵��ԭ���������ڿ���ѧ���ķ��������ͼ���������


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ƺ������ƾ�������DZͧ�еĹ����� | |
| B�� | ������������ȥ��ˮ������������������ | |
| C�� | �����������������ͻ����� | |
| D�� | ̼�����ƿ���������θ������ҩ�PʳƷ���ͼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �¶�130�桢ѹǿ3.03��105Pa | B�� | �¶�25�桢ѹǿ1.01��105Pa | ||
| C�� | �¶�130�桢ѹǿ5.05��105Pa | D�� | �¶�0�桢ѹǿ5.05��105Pa |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
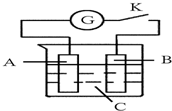 ��ͼ��ʾ����A��B����C����Һ�У��պϵ��K�������G��ָ��ᷢ��ƫת����B�������ݲ�������A��B��C�������ʿ����ǣ�������
��ͼ��ʾ����A��B����C����Һ�У��պϵ��K�������G��ָ��ᷢ��ƫת����B�������ݲ�������A��B��C�������ʿ����ǣ�������| A�� | A��Cu��B��Zn��C��CuSO4��Һ | B�� | A��Cu��B��Cu��C��H2SO4��Һ | ||
| C�� | A��Zn��B��ʯī��C��ϡH2SO4��Һ | D�� | A��ʯī��B��Zn��C��CuSO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �ɢ��֪X��һ������SiO2 | B�� | ���жϻ�������Ƿ���Na2O | ||
| C�� | 1.92 g����ɷ�ΪCu | D�� | 15.6 g�����X��m��Fe2O3����m��Cu��=1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | �缫���� | �������Һ | ������ָ��ƫת���� |
| 1 | Al��Mg | ϡ���� | ƫ��Al |
| 2 | Al��Cu | ϡ���� | ƫ��Cu |
| 3 | Al��ʯī | ϡ���� | ƫ��ʯī |
| 4 | Al��Mg | �������� | ƫ��Mg |
| 5 | Al��Zn | Ũ���� | ƫ��Al |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڱ�״���£�22.4LCH4��18gH2O�����еĵ�������Ϊ10 NA | |
| B�� | 2.3 g����������������ȼ�գ���ʧȥ�ĵ�����Ϊ0.2NA | |
| C�� | ��״���£�2g��������ԭ����ĿΪNA | |
| D�� | 100mL0.2mol/L BaCl2��Һ��Cl-����ĿΪ0.02NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������۵�ߴ�2045�棬�������Ƴ������ۻ��������ƹ��� | |
| B�� | HF�������ڿ�ʴ���� | |
| C�� | þ���Ͻ����������ɻ��IJ��� | |
| D�� | �������ƿ����������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com