
| 1 |
| 2 |
| 1 |
| 2 |
| 1mol×18g/mol |
| 1g |


科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
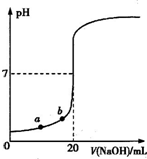
| A.水电离出的氢离子浓度:a>b |
| B.盐酸的物质的量浓度为0.0100mol?L-1?? |
| C.指示剂变色时,说明盐酸与NaOH恰好完全反应 |
| D.当滴加NaOH溶液10.00 mL(忽略反应前后体积变化),该混合液的pH=1+lg3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.32g | B.48g | C.56g | D.64g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-183kJ?mol-1 | B.-91.5kJ?mol-1 |
| C.+183kJ?mol-1 | D.+91.5kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.υ(D)=0.4mol?L-1?s-1 | B.υ(C)=0.5mol?L-1?s-1 |
| C.υ(B)=0.6mol?L-1?s-1 | D.υ(A)=2mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 K(g)+NaCl(l)
K(g)+NaCl(l) | A.②⑥ | B.①②③ | C.②⑤⑥ | D.①③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com