
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做()
A. 阴极 B. 阳极 C. 正极 D. 负极
科目:高中化学 来源: 题型:
用10mL的0.1mol•L﹣1 BaCl2溶液恰好可使相同体积的硫酸铁(Fe2(SO4)3)、硫酸锌(ZnSO4)和硫酸钾(K2SO4)三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
|
| A. | 3:2:2 | B. | 1:2:3 | C. | 1:3:3 | D. | 3:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和8体积氯气发生取代反应.由此可以断定原气态烃是(气体体积均在相同条件下测定)()
A. 乙炔 B. 丙炔 C. 2﹣戊炔 D. 1,3﹣丁二烯
查看答案和解析>>
科目:高中化学 来源: 题型:
某芳香化合物A分子式为C8H9Br(核磁共振氢谱显示五种不同信号,其面积之比为2:2:2:2:1),与NaOH的乙醇溶液共热后生成芳香烃B,B可与1molH2发生侧链上的加成反应得到苯的同系物C,芳香化合物A亦可与NaOH的水溶液共热后得到某醇D,D在一定条件下也可反应得到B.据此完成下列问题:
(1)分别写出由A生成B,由A生成D的化学方程式,并注明反应类型
A生成B ,
A生成D ,
(2)B在一定条件下可发生加聚反应生成重要的高分子化合物E,请写出该反应的化学方程式
(3)C的分子式为 ,C有多种同分异构体,请写出其含苯环的同分异构体的结构简式(不含C本身)
.
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将已知浓度的盐酸滴定到未知浓度的Na2CO3溶液,用pH传感器测得混合溶液的pH变化曲线,如图所示:(已知饱和CO2溶液的pH为5.6)下列说法正确的是()
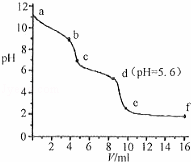
A. a点时,溶液呈碱性的原因是CO32﹣发生水解反应,其离子方程式为:CO32﹣+2H2O=H2CO3+2OH﹣
B. a→b段,溶液有气体放出
C. c点以后,盐酸过量
D. d点溶液中c(Na+)=c(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
关于原电池和电解池的叙述正确的是()
A. 原电池中失去电子的电极为阴极
B. 原电池的负极、电解池的阳极都发生氧化反应
C. 原电池的两极一定是由活动性不同的两种金属组成
D. 电解时电解池的阴极一定是阴离子放电
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,对于反应N2(g)+3H2(g)⇌2NH3(g)△H=﹣92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是()
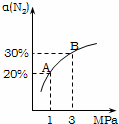
A. 将1.0mol氮气、3.0mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4kJ
B. 平衡状态由A变到B时,平衡常数K(A)<K(B)
C. 上述反应在达到平衡后,增大压强,H2的转化率提高
D. 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是()
A. CuCl2[CuSO4] B. NaOH[NaOH] C. NaCl[HCl] D. CuSO4[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
一元中强酸次磷酸(H3PO2)是一种精细化工产品,下列说法正确的是()
A. 次磷酸的电离方程式为H3PO2⇌3H++PO23﹣
B. 次 磷酸中P的化合价为+1
磷酸中P的化合价为+1
C. NaH2PO2是酸式盐
D. NaH2PO2溶液显弱酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com