
| A. | 10℃20 mL3mol/L的x溶液 | B. | 20℃30 mL2mol/L的x溶液 | ||
| C. | 10℃10 mL4mol/L的x溶液 | D. | 10℃20 mL2mol/L的x溶液 |
分析 先计算出稀释后X溶液的中X的物质的量,最后溶液的体积都为100mL,则物质的量越大,浓度越大,则反应速率越大;并结合温度越高,反应速率越大来判断.
解答 解:A.10℃20 mL3mol/L的X溶液,X的物质的量为0.02L×3mol/L=0.06mol,
B.20℃30 mL2mol/L的x溶液,X的物质的量为0.03L×2mol/L=0.06mol,
C、10℃10 mL4mol/L的X溶液,X的物质的量为0.01L×4mol/L=0.04mol,
D、10℃20 mL2mol/L的X溶液,X的物质的量为0.02L×4mol/L=0.04mol,
显然四种情况下B中温度最高,浓度最大,所以反应速率是最大,
故选B.
点评 本题考查反应速率与温度、浓度的关系及物质的量的计算,难度不大.明确影响化学反应速率的因素、物质的量与浓度的关系是解答本题的关键.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
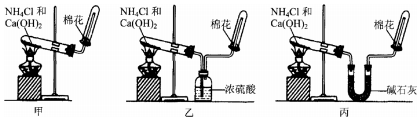
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n(Na+):n(Cl-) 可能为7:4 | |
| B. | 与NaOH反应的氯气一定为0.1mol | |
| C. | 若反应中转移的电子为n mol,则0.15<n<0.25 | |
| D. | n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40.75 | B. | 29.38 | C. | 14.69 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2分子由1个硅原子和2个氧原子组成 | |
| B. | 水晶的主要成分是单质硅 | |
| C. | 太阳能电池可采用SiO2制作,其应用有利于节能、环保 | |
| D. | 水玻璃可用作黏合剂和木材防火剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com