
| A. | 过滤 | B. | 蒸发 | C. | 蒸馏 | D. | 萃取 |
科目:高中化学 来源: 题型:推断题
 a、b、c、d、e、f是原子序数依次增大的6种短周期元素,a、d同主族,a是原子半径最小的元素,b的最高正化合价与最低负化合价的代数和为零,a与c、d与c均可形成原子个数之比为2:1和1:1的化合物,d、e的最外层电子数之和等于b的最外层电子数,f是同周期中得电子能力最强的元素.
a、b、c、d、e、f是原子序数依次增大的6种短周期元素,a、d同主族,a是原子半径最小的元素,b的最高正化合价与最低负化合价的代数和为零,a与c、d与c均可形成原子个数之比为2:1和1:1的化合物,d、e的最外层电子数之和等于b的最外层电子数,f是同周期中得电子能力最强的元素. .a、c、d三种元素形成的化合物中存在的化学键类型是离子键、共价键.
.a、c、d三种元素形成的化合物中存在的化学键类型是离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:6 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | Cl2的水溶液能导电,所以Cl2是电解质 | |
| B. | 用铂丝蘸取NaCl溶液进行焰色反应是化学变化 | |
| C. | 除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸 | |
| D. | 按照如图操作,配制0.10 mol•L-1 NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 元素性质或原子结构 |
| T | 元素最高正价是+6 |
| X | 在短周期元素中原子半径最大 |
| Y | 氢化物与最高价氧化物对应的水化物反应生成盐 |
| Z | M层上有7个电子 |
| W | 其单质既能跟酸反应,又能跟碱反应,且都产生H2 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
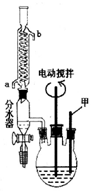 苯甲酸(C6H5COOH式量:122,熔点122.4℃,密度为1.2659g•cm-3)是一种一元有机弱酸,微溶于水易溶于乙醇.实验室中由甲苯(式量:92,密度为0.8669g•cm-3)制备苯甲酸的实验如下:
苯甲酸(C6H5COOH式量:122,熔点122.4℃,密度为1.2659g•cm-3)是一种一元有机弱酸,微溶于水易溶于乙醇.实验室中由甲苯(式量:92,密度为0.8669g•cm-3)制备苯甲酸的实验如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林可浸制标本,因其可使蛋白质变性的性质 | |
| B. | 向牛奶中加入果汁会产生沉淀,这是因为发生了酸碱中和反应 | |
| C. | 将地沟油制成肥皂,可以提高资源的利用率 | |
| D. | 用CO2合成聚碳酸酯可降解塑料,实现碳的循环利用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com