
| A. | 质量相等,密度不等的N2和C2H4两种气体含有的分子数一定相等 | |
| B. | 同温同压下,等体积的H2和He气含有的质子数相等 | |
| C. | 某物质经分析仅含一种元素,此物质可能是纯净物也可能是混合物 | |
| D. | FeCl3溶液呈电中性,Fe(OH)3胶体带有电荷 |
分析 A.根据n=$\frac{m}{M}$可知,相等质量氮气、乙烯的物质的量相等,故二者含有分子数目相等;
B.同温同压下,等体积的H2和He的物质的量相等,每个分子均含有2个质子;
C.同种元素组成的物质可能互为同素异形体;
D.Fe(OH)3胶体不带电.
解答 解:A.氮气、乙烯的摩尔质量相等,根据n=$\frac{m}{M}$可知,相等质量氮气、乙烯的物质的量相等,故二者含有分子数目相等,故A正确;
B.同温同压下,等体积的H2和He的物质的量相等,氦气为单原子分子,每个分子均含有2个质子,则含有质子数相等,故B正确;
C.由于同种元素组成的物质可能互为同素异形体,含一种元素的物质可能是纯净物也可能是混合物,故C正确;
D.Fe(OH)3胶体胶粒带正电荷,但胶体不带电,故D错误,
故选D.
点评 本题考查物质的量有关计算、基本概念、胶体性质等,比较基础,注意对基础知识的理解掌握.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol固态物质或液态物质的体积主要决定于构成这种物质的粒子的大小 | |
| B. | 在相同温度和压强下,任何气体粒子之间的距离可看成相等的 | |
| C. | 某同学用容量瓶配制溶液加水时不慎超出刻度线必须重新配制 | |
| D. | 为与容量瓶的精度相匹配称量固体质量时应用托盘天平 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10g 46%的乙醇溶液所含氢原子数为1.2NA | |
| B. | 0.5 mol熔融的NaHSO4中含有的离子数目为1.5NA | |
| C. | 标准状况下,2.24L甲醇中含有C-H键的数目为0.3NA | |
| D. | S2和S8的混合物共38.4g,其中所含硫原子数为1.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
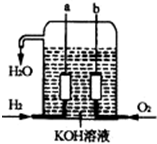 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 化学变化中的能量变化主要是由化学键变化引起的 | |
| C. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| D. | 能量变化是化学反应的基本特征之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
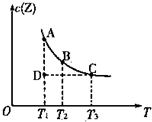 在容积不变的密闭容器中有反应:X(g)+Y(g)?Z(g),若Z(g)的物质的量浓度c(Z)与温度T的关系如图所示(曲线上的任意一点都表示平衡状态).则下列说法不正确的是( )
在容积不变的密闭容器中有反应:X(g)+Y(g)?Z(g),若Z(g)的物质的量浓度c(Z)与温度T的关系如图所示(曲线上的任意一点都表示平衡状态).则下列说法不正确的是( )| A. | A点与B点相比,B点的c(X)大 | B. | A点与C点的化学反应速率:A<C | ||
| C. | 在反应进行到D点时,v正>v逆 | D. | 该反应的正反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | A | B | C | D |
| n(CO2)(mo1) | 1 | 2 | 3 | 4 |
| n(沉淀)(mo1) | 1 | 1 | 2 | 2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com