
| A. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=+817.63 kJ•mol-1 | |
| B. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63 kJ•mol-1 | |
| C. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(l)△H=-641.63 kJ•mol-1 | |
| D. | N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-817.63 kJ•mol-1 |
分析 已知:①N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=-533.23kJ•mol-1
②H2O(g)=H2O (l)△H2=-44kJ•mol-1
②2H2O2(l)=2H2O(l)+O2(g)△H3=-196.4kJ•mol-1,
根据盖斯定律,将①+③-②可得N2H4(g)+2H2O2(l)═N2(g)+4H2O(g),据此计算出该反应的焓变△H即可.
解答 解:已知:①N2H4(g)+O2(g)=N2(g)+2H2O(g)△H1=-533.23kJ•mol-1
②H2O(g)=H2O (l)△H2=-44kJ•mol-1
②2H2O2(l)=2H2O(l)+O2(g)△H3=-196.4kJ•mol-1,
根据盖斯定律,将①+③-②可得:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=(-533.23kJ•mol-1)+(-196.4kJ•mol-1)-(-44kJ•mol-1)=-641.63 kJ•mol-1,
故选B.
点评 本题考查了盖斯定律在热化学方程式中的应用,题目难度中等,明确盖斯定律的含义及应用方法为解答关键,注意掌握热化学方程式的书写原则,试题培养了学生的灵活应用能力.


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同质量不同密度的C2H4和CO | B. | 同温度同体积的C2H6和NO2 | ||
| C. | 同温度同密度的CO2和N2 | D. | 同体积同压强的N2和C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾一淀粉试纸检验,观察试纸颜色的变化 | |
| B. | 铝热剂溶于足量稀盐酸再滴加KSCN溶液,未出现血红色,该铝热剂不含氧化铁 | |
| C. | 测氯水的pH可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较 | |
| D. | 向硅酸钠溶液中,滴入硫酸,可以验证S的非金属性强于Si |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅是良好的半导体材料 | |
| B. | 硅用于光导纤维 | |
| C. | SiO2不溶于水,也不溶于任何酸 | |
| D. | 用带玻璃瓶塞的试剂瓶盛放NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油 | |
| B. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 | |
| C. | 煤干馏和石油分馏本质差别是:干馏是化学变化而分馏是物理变化 | |
| D. | 煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KH的水溶液呈碱性 | B. | KH中氢离子可以被还原为氢气 | ||
| C. | KH是一种强氧化剂 | D. | KH中的氢离子是裸露的质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
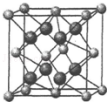 氟在自然界中常以CaF2的形式存在.
氟在自然界中常以CaF2的形式存在.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com