
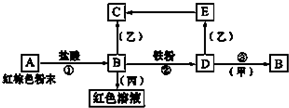
 下列物质之间有如图反应关系:已知由E转化成C的现象是灰白色沉淀迅速变为灰绿色,最后变为红褐色.回答:
下列物质之间有如图反应关系:已知由E转化成C的现象是灰白色沉淀迅速变为灰绿色,最后变为红褐色.回答:

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 应量取盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生物柴油具有良好的燃料性能,且安全、环保、可再生,它的成分是高级脂肪酸甲酯或乙酯 |
| B、PM2.5的颗粒物,分散在空气中可形成胶体 |
| C、制造生活中的水杯、奶瓶、食物保鲜膜等,使用聚乙烯材料比聚氯乙烯更有利于健康 |
| D、甘油与汽油都不属于化学意义上的油 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com