
 浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C
浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C
| ||
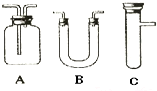
| 选用的仪器 (填字母) | 加入的试剂 | 作用 |
| C | 浓H2SO4、木炭 | 发生反应 |
| B | 检验产物水 | |
| A | 检验SO2 | |
| A | 酸性KMnO4溶液 | |
| A | 品红 | |
| A | 检验CO2的存在 |
| ||
| ||
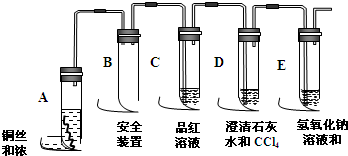
| 选用的仪器 (填字母) | 加入的试剂 | 作用 |
| C | 浓H2SO4、木炭 | 发生反应 |
| B | 无水CuSO4 | 检验产物水 |
| A | 品红溶液 | 检验SO2 |
| A | 酸性KMnO4溶液 | 吸收余下的SO2 |
| A | 品红 | 检验SO2是否除尽 |
| A | 澄清石灰水 | 检验CO2的存在 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
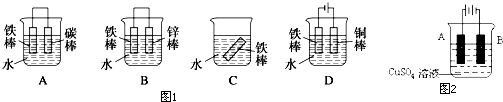
| A、1:3 | B、3:1 |
| C、3:2 | D、1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60s |
| 褪色后,再滴入第2滴 | 15s |
| 褪色后,再滴入第3滴 | 3s |
| 褪色后,再滴入第4滴 | 1s |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述四种氧化物对应的水化物中,至少有三种是碱性氧化物 |
| B、将固体X加入氢氟酸中,X会溶解 |
| C、滤液Y中的阳离子只有Mg2+、Al3+、Fe3+三种 |
| D、滤液Y中加入过量氨水,所得沉淀为Fe(OH)3和Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
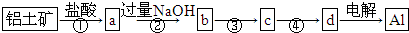
| A、①②中除加试剂外,还需要进行过滤操作 |
| B、a、b中铝元素的化合价不相同 |
| C、③中需要通入过量的CO2 |
| D、④进行的操作是加热,而且d一定是氧化铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com