
| A. | X、M两种元素形成的化合物中只能存在离子键 | |
| B. | 元素Z的某种氧化物具有漂白性,是因为这种氧化物具有强氧化性 | |
| C. | 由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 | |
| D. | 元素W和M的某些单质可作为水处理中的消毒剂 |
分析 有M、X、Y、Z、W五种原子序数依次增大的短周期主族元素,Y的单质晶体熔点高、硬度大,是一种重要的半导体材料可知Y为Si;由X+与M2-具有相同的电子层结构,可知X为Na、M为O;Z、M同主族,则Z为S;离子半径Z2->W-,则W为Cl,结合原子序数可知X只能为F,然后结合元素周期律来解答.
解答 解:有M、X、Y、Z、W五种原子序数依次增大的短周期主族元素,Y的单质晶体熔点高、硬度大,是一种重要的半导体材料可知Y为Si;由X+与M2-具有相同的电子层结构,可知X为Na、M为O;Z、M同主族,则Z为S;离子半径Z2->W-,则W为Cl,结合原子序数可知X只能为F,
A.X、M两种元素形成的化合物若为过氧化钠,含离子键和共价键,故A错误;
B.Z的某种氧化物二氧化硫具有漂白性,是因与有色物质化合生成无色物质,故B错误;
C.W的氢化物分子间含氢键,沸点最高,而Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低,故C错误;
D.元素W和M的某些单质(氯气、臭氧),均具有强氧化性,氯气与水反应生成的HClO具有强氧化性,可作为水处理中的消毒剂,故D正确;
故选D.
点评 本题考查位置、结构及性质的综合应用,为高频考点,把握元素的位置、元素的性质、原子结构推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识及周期律的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
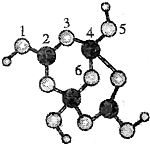 硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:下列叙述正确的是( )
硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:下列叙述正确的是( )| A. | Xm-的化学式为B4O8H42- | |
| B. | 硼原子轨道的杂化类型有sp2、sp3 | |
| C. | 配位键存在于4、6原子之间 | |
| D. | 硼砂晶体中有离子键、配位键两种化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的漂白原理与次氯酸相同 | B. | 硫在足量空气中燃烧生成大量SO3 | ||
| C. | 浓硫酸可以干燥H2、H2S、CO2等气体 | D. | 可用铝槽储运浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、CCl4、C60都是含有极性键的非极性分子 | |
| B. | 非金属氢化物的稳定性顺序:H2O>H2S>H2Se,HCl<H2S<PH3 | |
| C. | 弱电解质水溶液导电能力不一定比强电解质水溶液导电能力弱 | |
| D. | 空间利用率:简单立方堆积<体心立方堆积<六方最密堆积<面心立方最密堆积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含1molNa2CO3的溶液中CO32-的微粒数目 | |
| B. | 常温常压下,22.4 L N2的原子数目 | |
| C. | 46gNO2和N2O4的混合气体中的原子数 | |
| D. | 28g铁在反应中作还原剂时,失去电子的数目 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫原子的原子结构示意图: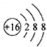 | |
| B. | NH4Cl的电子式: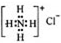 | |
| C. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| D. | 用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
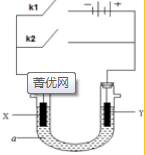 原电池与电解池在化学工业中有广泛应用.如图装置,a为CuCl2溶液,X为Fe棒,Y为碳棒,回答以下问题:
原电池与电解池在化学工业中有广泛应用.如图装置,a为CuCl2溶液,X为Fe棒,Y为碳棒,回答以下问题: Fe2+;电解质溶液中的阳离子向Y极移动(填X或Y);
Fe2+;电解质溶液中的阳离子向Y极移动(填X或Y);查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以烽燧铳极”这是利用了“KNO3的氧化性” | |
| B. | 李白有诗云“日照香炉生紫烟”这是描写“碘的升华” | |
| C. | 《本草经集注》中记载了区分硝石(KNO3)和朴消(Na2SO4)的方法:“以火烧之,烟起,乃真硝石也”这是利用了“焰色反应” | |
| D. | 我国古代人民常用明矾除去铜器上的铜锈[Cu2(OH)2CO3] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com