
| A. | BaSO3与BaSO4沉淀 | B. | BaSO3沉淀 | ||
| C. | BaSO4沉淀 | D. | 无法得到沉淀物 |
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:解答题
| 需加入的试剂 | 分离装置 | |
| 乙烷(乙烯) | c | D |
| 溴苯(液溴) | b | A |
| 苯(苯酚) | b | A |
| 乙醇(水) | e | C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.045mol/L | B. | 0.036mol/L | C. | 0.026mol/L | D. | 0.030mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量的氨气:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 浓烧碱溶液中加入铝片:Al+2OH+H2O═AlO2-+H2↑ | |
| C. | 用浓NaOH溶液溶解Al2O3:Al2O3+2OH═2AlO2-+H2O | |
| D. | 向NaAlO2溶液中通入过量的CO2:2AlO2+CO2+3H2O═Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C5H12 | C. | C8H18 | D. | C9H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①②③ | B. | 只有①②④⑤ | C. | 只有①②④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
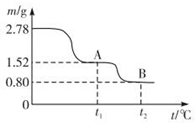 在中国古代,炼丹家以绿矾(FeSO4•7H2O为原料,放在炼丹炉中锻烧可制得绿矾油.绿矾油是一种无色粘稠液体,可用于除掉兵器上的铁锈.如图是2.78g绿矾隔绝空气受热分解时,所得固体产物的质量随温度变化的曲线.将加热产生的所有气体通入足量的BaCl2溶液.得自色沉淀1.16g.
在中国古代,炼丹家以绿矾(FeSO4•7H2O为原料,放在炼丹炉中锻烧可制得绿矾油.绿矾油是一种无色粘稠液体,可用于除掉兵器上的铁锈.如图是2.78g绿矾隔绝空气受热分解时,所得固体产物的质量随温度变化的曲线.将加热产生的所有气体通入足量的BaCl2溶液.得自色沉淀1.16g.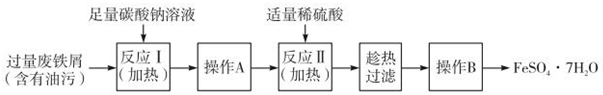
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上10月月考化学试卷(解析版) 题型:填空题
(1)如图所示,若C为浓硝酸,电流表指针发生偏转,B电极材料为Fe ,A电极材料为Cu,则B电极的电极反应式为______________,A电极的电极反应式为 ;反应进行一段时间后溶液C的pH将 (填“升高”“降低”或“ 基本不变”)。
基本不变”)。
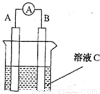
(2)我国首创以铝空气海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流 ,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是________,负极反应为___________;正极反应为_______________________。
,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是________,负极反应为___________;正极反应为_______________________。
(3)熔盐电池具有高的发电效率,因而受到重视, 可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池,完成有关电池反应式。负极反应式为2CO+2CO32-4e-=4CO2,正极反应式为________________________,电池总反应式为_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com