
N2O5ŹĒŅ»ÖÖŠĀŠĶĻõ»Æ¼Į£¬ŌŚŅ»¶ØĪĀ¶ČĻĀæÉ·¢ÉśŅŌĻĀ·“Ó¦£ŗ2N2O5(g) 4NO2(g)£«O2(g) ¦¤H£¾0£¬T1ĪĀ¶ČŹ±£¬ĻņĆܱÕČŻĘ÷ÖŠĶØČėN2O5£¬²æ·ÖŹµŃ鏿¾Ż¼ūĻĀ±ķ£¬ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ
4NO2(g)£«O2(g) ¦¤H£¾0£¬T1ĪĀ¶ČŹ±£¬ĻņĆܱÕČŻĘ÷ÖŠĶØČėN2O5£¬²æ·ÖŹµŃ鏿¾Ż¼ūĻĀ±ķ£¬ĻĀĮŠĖµ·ØÖŠ²»ÕżČ·µÄŹĒ
t/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/(mol”¤L£1) | 5.00 | 3.52 | 2.50 | 2.50 |
A£®500 sÄŚN2O5·Ö½āĖŁĀŹĪŖ2.96”Į10£3mol”¤L£1”¤s£1
B£®T1ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżK1£½125
C£®T1ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżĪŖK1£¬T2ĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżĪŖK2£¬ČōT1£¾T2£¬ŌņK1£¼K2
D£®“ļĘ½ŗāŗóĘäĖūĢõ¼ž²»±ä£¬½«ČŻĘ÷µÄĢå»żŃ¹Ėõµ½ŌĄ“µÄ1/2£¬ŌņŌŁ“ĪĘ½ŗāŹ±c(N2O5)£¾5.00 mol”¤L£1
C
”¾½āĪö”æ
ŹŌĢā½āĪö£ŗ500 sÄŚN2O5·Ö½āĖŁĀŹĪŖ(5.00-3.52)mol/L”Ā500s=2.96Øw10-3mol/( L”¤s)£¬¹ŹAÕżČ·£»·ÖĪö±ķÖŠŹż¾Ż£¬µĆ£ŗ1000 sŹ±“ļĘ½ŗā£¬ø÷ĪļÖŹµÄĘ½ŗāÅØ¶Č·Ö±šĪŖ2.5 mol”¤L£1”¢5.0 mol”¤L£1”¢1.25 mol”¤L£1£¬ŌņK1£½([NO2]4[O2])/[N2O5]2£½125£¬¹ŹBÕżČ·£»ÓÉÓŚøĆ·“Ó¦µÄÕż·“Ó¦ŹĒøöĘųĢåĢå»żŌö“óµÄĪüČČ·“Ó¦”£ĖłŅŌøł¾ŻĘ½ŗāŅʶÆŌĄķ£ŗÉżøßĪĀ¶Č£¬»ÆŃ§Ę½ŗāĻņĪüČČ·“Ó¦·½ĻņŅĘ¶Æ”£¶ŌøĆ·“Ó¦Ą“Ėµ¾ĶŹĒŹĒøöĪĀ¶Č£¬»ÆŃ§Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ”£Ę½ŗāŌ½ÕżĻņŅĘ¶Æ£¬Éś³ÉĪļµÄÅØ¶Č¾ĶŌ½“󣬷“Ó¦ĪļµÄÅØ¶Č¾ĶŌ½Š”£¬ĖłŅŌĘ½ŗā³£Źż¾ĶŌ½“ó”£Ņņ“ĖT1>T2£¬ŌņK1>K2£¬¹ŹC“ķĪ󣻓ļĘ½ŗāŗóĘäĖūĢõ¼ž²»±ä£¬½«ČŻĘ÷µÄĢå»żŃ¹Ėõµ½ŌĄ“µÄ1/2£¬¼“Ōö“óĮĖŃ¹Ē棬¼ŁČēĘ½ŗā²»·¢ÉśŅĘ¶Æ£¬c(N2O5)ŹĒŌĄ“µÄ2±¶£¬Ņ²¾ĶŹĒ5.00 mol/L.¶ųŌö“óŃ¹Ē棬»ÆŃ§Ę½ŗāÄęĻņŅĘ¶Æ£¬c(N2O5)Ōö“ó£¬ĖłŅŌc(N2O5)> 5.00 mol/L£¬¹ŹDÕżČ·”£
æ¼µć£ŗ»Æѧ·“Ó¦ĖŁĀŹŗĶ»ÆŃ§Ę½ŗā



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĖÄ“ØŹ”øßČżµŚČż“ĪĄķ×Ūæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø15·Ö£©¹č»łĢ«Ńōµē³ŲŠčÓĆ»ÆŗĻĪļ¼××÷¶Ū»Æ²ÄĮĻ£¬¼×µÄĦ¶ūÖŹĮæĪŖ140 g”¤mol£1£¬ĘäÖŠ¹čŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ60%”£ŅŃÖŖ1 molNH3Óė×ćĮæµÄ»ÆŗĻĪļŅŅ³ä·Ö·“Ó¦ŗóæɵƵ½35 g ¼×Óė6 g H2”£¹¤ŅµÉĻÖĘŅŅµÄĮ÷³ĢČēĻĀ£ŗ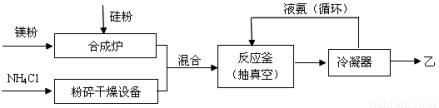 Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŅŅµÄµē×ÓŹ½ŹĒ £»±Č½ĻČČĪČ¶ØŠŌ£ŗŅŅ_______NH3£ØĢī£¾£¬£¼»ņ£½£©”£
£Ø2£©NH3Óė×ćĮæµÄ»ÆŗĻĪļŅŅ·“Ó¦ÖĘ¼×µÄ»Æѧ·½³ĢŹ½ŹĒ ”£
£Ø3£©ŗĻ³ÉĀÆÄŚĪļÖŹŠčŌŚ±£»¤Ęų·ÕĻĀøßĪĀŗĻ³É£¬ĻĀĮŠĘųĢåæÉ×÷±£»¤ĘųµÄÓŠ £ØĢī×ÖÄø±ąŗÅ£©”£
A£®O2 B£®H2 C£®N2 D£®CO2 E£®Ar
£Ø4£©ÉĻŹöÉś²śŅŅµÄ¹ż³ĢÖŠŅŗ°±µÄ×÷ÓĆŹĒ______________________________________”£
£Ø5£©¼×ÓėÉŁĮæH2SO4ČÜŅŗ·“Ó¦Ö»µĆµ½H2SiO3ŗĶŃĪMĮ½ÖÖ²śĪļ£¬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ ”£ĒėÉč¼ĘŃéÖ¤²śĪļŃĪMµÄŹµŃé·½°ø ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĖÄ“ØŹ”ĆąÖńŹŠøßČżÉĻѧʌµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖµ„ÖŹĢśČÜÓŚŅ»¶ØÅØ¶ČµÄHNO3ČÜŅŗÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ
aFe+bNO3©+cH+ ØT dFe2++fFe3++gNO”ü+hN2O”ü+kH2O£¬
»Æѧ¼ĘĮæŹża”«k¾łĪŖÕżÕūŹż£®ŌņĖüĆĒÖ®¼äµÄ¹ŲĻµ“ķĪóµÄŹĒ
A£®c=4g+10h B£®a+c=d+f
C£®2d+3f=3g+8h D£®c©b=2d+3f
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĖÄ“ØŹ”øßČż£Ø²¹Ļ°°ą£©10ŌĀŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijČÜŅŗÖŠŗ¬ÓŠ“óĮæµÄĻĀĮŠĄė×Ó£ŗFe3£«”¢SO42£”¢Al3£«ŗĶMĄė×Ó£¬¾²ā¶ØFe3£«”¢SO42£”¢Al3£«ŗĶM Ąė×ÓµÄĪļÖŹµÄĮæÖ®±ČĪŖ2”Ć4”Ć1”Ć1£¬ŌņMĄė×ÓæÉÄÜŹĒĻĀĮŠÖŠµÄ
A”¢Na£« B”¢Cl£ C”¢OH£ D”¢S2£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĖÄ“ØŹ”³É¶¼øߊĀĒųøßČż11ŌĀĶ³Ņ»¼ģ²ā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
£Ø12·Ö£©Ä³»Æѧ»ī¶ÆŠ”×éÉč¼ĘČēĶ¼ĖłŹ¾(²æ·Ö¼Š³Ö×°ÖĆŅŃĀŌČ„)ŹµŃé×°ÖĆ£¬ŅŌĢ½¾æ³±ŹŖµÄCl2ÓėNa2CO3·“Ó¦µĆµ½µÄ¹ĢĢåĪļÖŹ”£
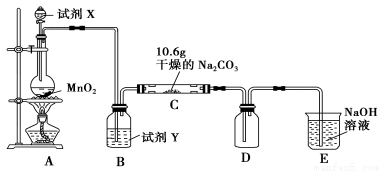
£Ø1£©Š“³ö×°ÖĆAÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø2£©Š“³öŹŌ¼ĮYµÄĆū³Ę£ŗ ”£
£Ø3£©ŅŃÖŖ£ŗĶØČėŅ»¶ØĮæµÄĀČĘųŗ󣬲āµĆDÖŠÖ»ÓŠŅ»ÖÖ³£ĪĀĻĀĪŖ»Ę×ŲÉ«µÄĘųĢ壬ĘäĪŖŗ¬ĀČŃõ»ÆĪļ”£æÉŅŌČ·¶ØµÄŹĒCÖŠŗ¬ĀČ»ÆŗĻĪļ(ŃĪ)Ö»ÓŠŅ»ÖÖ£¬ĒŅŗ¬ÓŠNaHCO3£¬ĻÖ¶ŌCµÄ³É·Ö½ųŠŠ²ĀĻėŗĶĢ½¾æ”£
¢ŁĢį³öŗĻĄķ¼ŁÉč”£
¼ŁÉč1£ŗ“ęŌŚĮ½Öֳɷ֣ŗNaHCO3ŗĶ £»
¼ŁÉč2£ŗ“ęŌŚČżÖֳɷ֣ŗNaHCO3ŗĶ ”¢ ”£
¢ŚÉč¼Ę·½°ø£¬½ųŠŠŹµŃ锣ĒėŠ“³öŹµŃé²½ÖčŅŌ¼°Ō¤ĘŚĻÖĻóŗĶ½įĀŪ(æɲ»ĢīĀś)”£
ĻŽŃ”ŹµŃéŹŌ¼ĮŗĶŅĒĘ÷£ŗÕōĮóĖ®”¢Ļ”HNO3”¢BaCl2ČÜŅŗ”¢³ĪĒåŹÆ»ŅĖ®”¢AgNO3ČÜŅŗ”¢ŹŌ¹Ü”¢Š”ÉÕ±”£
ŹµŃé²½Öč | Ō¤ĘŚĻÖĻóŗĶ½įĀŪ |
²½Öč1£ŗČ”CÖŠµÄÉŁĮæ¹ĢĢåѳʷӌŹŌ¹ÜÖŠ£¬µĪ¼Ó×ćĮæÕōĮóĖ®ÖĮ¹ĢĢåČܽā£¬Č»ŗó½«ĖłµĆČÜŅŗ·Ö±šÖĆÓŚa”¢bŹŌ¹ÜÖŠ”£ |
|
²½Öč2£ŗ | Ēéæö¢Ł£ŗ Ēéæö¢Ś£ŗ |
²½Öč3£ŗ |
|
£Ø4£©DÖŠ»Ę×ŲÉ«µÄĘųĢå»ÆѧŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĖÄ“ØŹ”³É¶¼øߊĀĒųøßČż11ŌĀĶ³Ņ»¼ģ²ā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲŹµŃé²Ł×÷”¢ĻÖĻóŗĶ½āŹĶ»ņ½įĀŪ¶¼ÕżČ·µÄŹĒ
A£®¹żĮæµÄFe·ŪÖŠ¼ÓČėĻ”HNO3£¬³ä·Ö·“Ó¦ŗ󣬵ĪČėKSCNČÜŅŗ£¬ČÜŅŗ³ŹŗģÉ«£¬ĖµĆ÷Ļ”HNO3½«FeŃõ»ÆĪŖFe3+
B£®Ä³¼ŲŃĪČÜÓŚŃĪĖį£¬²śÉśĪŽÉ«ĪŽĪ¶ĘųĢ壬Ķعż³ĪĒåŹÆ»ŅĖ®£¬ÓŠ°×É«³Įµķ³öĻÖ£¬ĖµĆ÷øĆ¼ŲŃĪŹĒK2CO3
C£®Al²²åČėĻ”HNO3ÖŠ£¬ĪŽĻÖĻó£¬ĖµĆ÷Al²±ķĆę±»HNO3Ńõ»Æ£¬ŠĪ³ÉÖĀĆܵÄŃõ»ÆĤ
D£®ÓĆ²£Į§°ōÕŗČ”ÅØ°±Ė®µćµ½ŗģÉ«ŹÆČļŹŌÖ½ÉĻ£¬ŹŌÖ½±äĄ¶É«£¬ÅØ°±Ė®³Ź¼īŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĖÄ“ØŹ”³É¶¼øߊĀĒųøßČż11ŌĀĶ³Ņ»¼ģ²ā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ¶ŌŅ»Š©ŹµŃéŹĀŹµµÄĄķĀŪ½āŹĶÕżČ·µÄŹĒ
| ŹµŃéŹĀŹµ | ĄķĀŪ½āŹĶ |
A | SO2ČÜÓŚĖ®ŠĪ³ÉµÄČÜŅŗÄܵ¼µē | SO2ŹĒµē½āÖŹ |
B | °×Į×ĪŖÕżĖÄĆęĢå·Ö×Ó | °×Į×·Ö×ÓÖŠP”ŖP¼äµÄ¼ü½ĒŹĒ109”ć28”ä |
C | 1Ģå»żĖ®æÉŅŌČܽā700Ģå»ż°±Ęų | °±ŹĒ¼«ŠŌ·Ö×Ó£»æÉÓėĖ®ŠĪ³ÉĒā¼ü£»ĒŅÓėĖ®·“Ó¦ |
D | HFµÄ·ŠµćøßÓŚHCl | H”ŖFµÄ¼ü³¤±ČH”ŖClµÄ¼ü³¤¶Ģ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ¼ŖĮÖŹ”³¤“ŗĶā¹śÓļѧŠ£øßČżÉĻѧʌʌ֊Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖHCN(aq)ÓėNaOH(aq)·“Ӧɜ³É1 molÕżŃĪµÄ¦¤H£½£12.1 kJ/mol£»ĒæĖį”¢Ēæ¼īµÄĻ”ČÜŅŗ·“Ó¦µÄÖŠŗĶČȦ¤H£½£57.3 kJ”¤mol£1”£ŌņHCNŌŚĖ®ČÜŅŗÖŠµēĄėµÄ¦¤HµČÓŚ
A£®+69.4 kJ”¤mol£1 B£®-69.4 kJ”¤mol£1
C£®+45.2 kJ”¤mol£1 D£®-45.2 kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ¼ŖĮÖŹ”øßČż10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ·“Ó¦£¬Ęä²śĪļŃÕÉ«°“ŗģÉ«”¢ŗģŗÖÉ«”¢µ»ĘÉ«”¢Ą¶É«Ė³ŠņÅÅĮŠµÄŹĒ( )
¢Ł½šŹōÄĘŌŚ“æŃõÖŠČ¼ÉÕ ¢ŚFeSO4ČÜŅŗÖŠµĪČėNaOHČÜŅŗ²¢ŌŚæÕĘųÖŠ·ÅÖĆŅ»¶ĪŹ±¼ä ¢ŪFeCl3ČÜŅŗÖŠµĪČėKSCNČÜŅŗ ¢ÜĪŽĖ®ĮņĖįĶ·ÅČėŅ½ÓĆ¾Ę¾«ÖŠ
A£®¢Ś¢Ū¢Ł¢Ü B£®¢Ū¢Ś¢Ł¢Ü C£®¢Ū¢Ł¢Ś¢Ü D£®¢Ł¢Ś¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com