
下列各组元素的所有组合中,既可形成离子化合物,又可形成共价化合物的是( )
A.H、C、O、K B.H、Na、O、S
C.H、N、O D.H、O、S
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
已知C3N4晶体具有比金刚石还大的硬度,且构成该晶体的微粒间只以单键结合。下列关于C3N4晶体的说法错误的是( )
A.该晶体属于原子晶体,其化学键比金刚石中的碳碳键更牢固
B.该晶体中每个碳原子连接4个氮原子、每个氮原子连接3个碳原子
C.该晶体中碳原子和氮原子的最外层都满足8电子结构
D.该晶体与金刚石相似,都是原子间以非极性键形成空间网状结构
查看答案和解析>>
科目:高中化学 来源: 题型:
有关A1型密堆积与A3型密堆积的说法中正确的是( )
A.A1型密堆积是最密堆积,A3型密堆积不是最密堆积
B.两者都是最密堆积,其中A3型密堆积是一、三、五……各层球心重合,二、四、六……各层球心重合;A1型密堆积是四、五、六各层球心分别和一、二、三层各球心重合
C.原子晶体一般都采用A1型密堆积或A3型密堆积
D.只有金属晶体才可能采用A1型密堆积或A3型密堆积
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关离子键的叙述中正确的是( )
①离子化合物中只含有离子键 ②共价化合物中可能含离子键 ③含离子键的化合物即为离子化合物
④共价化合物中不含离子键
A.①② B.②③
C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各选项的两个反应中属于同一反应类型的是( )
| 选项 | 反应Ⅰ | 反应Ⅱ |
| A | 在光照条件下,乙烷与溴蒸气反应制取CH3CH2Br | 将乙烯通入溴的四氯化碳溶液中制取1,2-二溴乙烷 |
| B | 在镍作催化剂的条件下,苯与氢气反应生成环己烷 | 在一定条件下,乙烯通过固体酸催化剂直接与水反应生成乙醇 |
| C | 在银作催化剂的条件下,乙醇与空气中的氧气反应生成乙醛 | 在一定条件下,由氯乙烯(CH2=CHCl)合成聚氯乙烯 |
| D | 乙酸乙酯在酸的催化作用下与水反应生成乙酸和乙醇 | 在一定条件下,液态植物油与氢气反应制人造脂肪 |
查看答案和解析>>
科目:高中化学 来源: 题型:
透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。以下是制备它的一种配方中含有的两种物质:
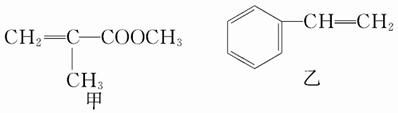
(1)甲中含有的官能团名称为____________。
(2)下列试剂能与甲反应而褪色的是______(填标号)。
a.溴的CCl4溶液 b.石蕊试液
c.酸性KMnO4溶液
(3)甲和乙两种物质均能发生的反应类型是______(填标号)。
a.取代反应 b.加成反应 c.酯化反应
d.加聚反应 e.水解反应 f.氧化反应
(4)写出下列反应的化学方程式:
①乙与溴的四氯化碳溶液反应_____________________;
②甲与NaOH溶液共热的反应______________________;
③由甲生成高分子化合物的反应___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
正误判断,正确的划“√”,错误的划“×”
(1)0.1 L 3.0 mol·L-1的NH4NO3溶液中含有的NH 的数目为0.3NA( )
的数目为0.3NA( )
(2)等体积、等物质的量浓度的NaCl和KCl溶液中,阴、阳离子数目之和均为2NA( )
(3)0.1 mol·L-1的NaHSO4溶液中,阳离子的数目之和为0.2NA( )
(4)25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA( )
查看答案和解析>>
科目:高中化学 来源: 题型:
用“偏大”、“偏小”或“无影响”填空
(1)配制450 mL 0.1 mol·L-1的NaOH溶液,用托盘天平称取NaOH固体1.8 g________。
(2)配制500 mL 0.1 mol·L-1的硫酸铜溶液,用托盘天平称取胆矾8.0 g________。
(3)配制NaOH溶液时,天平的两个托盘上放两张质量相等的纸片,其他操作均正确________。
(4)配制一定物质的量浓度的NaOH溶液,需称量溶质4.4 g,称量时物码放置颠倒________。
(5)用量筒量取浓硫酸时,仰视读数________。
(6)配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容________。
(7)定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线________。
(8)定容摇匀后,发现液面下降,继续加水至刻度线________________________________________________________________________。
(9)定容时仰视刻度线________。
(10)定容摇匀后少量溶液外流________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com