
| A、减压 | B、升温 |
| C、加入合适的催化剂 | D、增大B的浓度 |


科目:高中化学 来源: 题型:
| A、Cl2是氧化剂,反应中Cl原子得到电子 |
| B、当1molCl2完全反应时,有2mol电子发生转移 |
| C、NaBr是还原剂,反应中溴离子得到电子 |
| D、当1molNaBr完全反应时,有1mol电子发生转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 台湾的食品中“塑化剂”是一种塑料中的添加剂,不是食品添加剂,会危害男性生殖能力,促使女性性早熟,会伤害人类基因.因此不能用于食品当中,而且用了增塑剂的包装材料或者容器不能用于包装脂肪性的食品.有关说法正确的是( )
台湾的食品中“塑化剂”是一种塑料中的添加剂,不是食品添加剂,会危害男性生殖能力,促使女性性早熟,会伤害人类基因.因此不能用于食品当中,而且用了增塑剂的包装材料或者容器不能用于包装脂肪性的食品.有关说法正确的是( )| A、“塑化剂”能溶于水 |
| B、“塑化剂”是邻苯二甲酸酯,它水解可以生成邻苯二甲酸和醇 |
| C、该物质为高分子化合物 |
| D、应推广使用聚氯乙烯塑料袋包装食品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
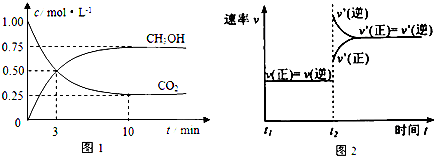
| 催化剂 |
| 加热、加压 |
| 物质 | CH3OH | CH3OCH3 | H2O |
| c/mol?L-1 | 0.44 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将淀粉与稀硫酸加热一段时间后,欲检验淀粉已经水解,可直接加入银氨溶液 |
B、有机物  的消去产物有两种 的消去产物有两种 |
| C、某有机化合物相对分子质量为109,将该化合物在强碱水溶液中水解后先用HNO3酸化,再用AgNO3溶液,结果生成淡黄色沉淀,则该有机物可能为C3H7Br |
| D、可用溴水鉴别甲苯、苯酚、1-己烯、淀粉碘化钾溶液、四氯化碳等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释溶液,水解程度减小 | ||||||
| B、通入CO2,平衡朝正反应方向移动 | ||||||
C、升高温度,
| ||||||
| D、加入NaOH固体,溶液PH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| B、某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| C、向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色,将SO2通入溴水,溴水褪色后加热也能恢复原色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com