
| 实验 序号 | 实验操作 | 实验现象 |
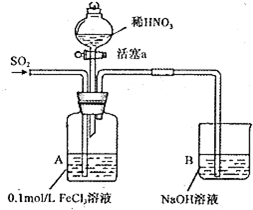
| I | 向A装置中通入一段时间的SO2气体. | A中黄色溶液最终变为浅绿色. |
| II | 取出少量A装置中的溶液,先加入 KSCN溶液,再加入BaCl2溶液. | 加人KSCN溶液后溶液不变色;再加入BaCl2溶液产生白色沉淀. |
| III | 打开活塞a,将过量稀HNO3加入装置A 中,关闭活塞a. | A中浅绿色溶液最终变为黄色. |
| V | 取出少量A装置中的溶液,加入KSCN 溶液. | 溶液变为红色. |
分析 (1)氯化铁中的铁离子具有氧化性,能将二氧化硫氧化为硫酸根,本身被还原为亚铁离子;
(2)硫酸根离子遇到钡离子会发生反应生成硫酸钡沉淀;
(3)硝酸能将亚铁离子氧化为铁离子,浅绿色溶液最终变为黄色;
(4)一氧化氮遇到空气会迅速变为红棕色;
(5)根据氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性来回答.
解答 解:(1)氯化铁中的铁离子具有氧化性,能将二氧化硫氧化为硫酸根,本身被还原为亚铁离子,发生反应:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(2)A装置中的溶液含有硫酸根离子,先加入 KSCN溶液,再加入BaCl2溶液,会发生反应产生白色沉淀,即Ba2++SO42-=BaSO4↓,
故答案为:Ba2++SO42-=BaSO4↓;
(3)A装置中的溶液含有亚铁离子,在酸性条件下,NO3-把Fe2+氧化为Fe3+,A中浅绿色溶液最终变为黄色,故答案为:在酸性条件下,NO3-把Fe2+氧化为Fe3+;
(4)A装置中的溶液含有亚铁离子,在酸性条件下,NO3-把Fe2+氧化为Fe3+,硝酸被还原为一氧化氮,一氧化氮遇到空气会迅速变为红棕色,所以液面上方气体由无色变为红棕色,故答案为:液面上方气体由无色变为红棕色;
(5)在酸性条件下,NO3-把Fe2+氧化为Fe3+,3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O,所以氧化性顺序是:NO3->Fe3+,根据反应:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,得到氧化性顺序是:Fe3+>SO42-,综上得到在酸性条件下,氧化性强弱顺序为NO3->Fe3+>SO42-,
故答案为:NO3->Fe3+>SO42-.
点评 本题考查了物质性质的实验分析判断,物质性质和离子检验,注意氧化还原反应的分析应用,掌握基础是解题关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mL pH=2 的醋酸溶液加水稀释到10mL,pH 变为3 | |
| B. | 常温下,Na2CO3溶液中加水稀释时,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$增大 | |
| C. | 向氯水中加入少量NaOH 溶液,一定有c(Na+)=c(Cl-)+c(ClO-) | |
| D. | NH4Cl 溶液稀释过程中,c(NH4+)与c(NH3•H2O)之和始终保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| H2O | H2S | H2Se | H2Te |
| 100℃ | -60.75℃ | -41.5℃ | -1.8℃ |
| A. | 氧族元素氢化物沸点高低与范德华力的大小无关 | |
| B. | 范德华力一定随相对分子质量的增大而减小 | |
| C. | 水分子间可能还存在一种特殊的分子间作用力 | |
| D. | 水分子间存在共价键,加热时较难断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢能、核能均是无污染的高效能源 | |
| B. | 公共汽车大部分采用天然气作为燃料可减少对大气的污染 | |
| C. | 把煤转化为液态燃料可提高煤的燃烧效率 | |
| D. | 使用催化剂,能增大活化分子百分数,所以反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z |
| A. | 氧、磷、氯 | B. | 氮、硅、硫 | C. | 氟、硫、氩 | D. | 碳、铝、磷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com