

 实验操作 实验操作 | 预期的现象及结论 |
| 步骤1:取1mL0.1mol/L Na2SO3和1mL0.1mol/L KI溶液于试管中,混合后滴入2~3滴新制氯水,振荡。 | |
| 步骤2:____________________________ _____________________________________ | ____________________________________ _______________________________________ |
 步骤3:取1mL0.1mol/L KI和1mL0.1mol/LFeCl2溶液于试管中,混合后滴入2~3滴新制氯水,振荡。 步骤3:取1mL0.1mol/L KI和1mL0.1mol/LFeCl2溶液于试管中,混合后滴入2~3滴新制氯水,振荡。 | |
| 步骤4:____________________________ _____________________________________ | ____________________________________ _______________________________________ |
| 实验操作 | 预期现象与结论 |
| 步骤2:向试管中加入足量的 1 mol·L-1HCl 后再滴入数滴(少许) 1 mol·L-1BaCl2,振荡试管 | 若没有白色沉淀产生,则说明还原性:I—>SO32— 或:若没有白色沉淀产生,则说明假设2不成立 或:若没有白色沉淀产生,则说明假设1成立 |
| 步骤2:(方法2)向试管中滴入少量淀粉溶液,振荡试管 | 若不变蓝色,说明还原性:SO32—>I— 或:若变蓝色,说明还原性:I—>SO32— |
| 步骤4:(方法1)向试管中滴入少量淀粉溶液 ,振荡试管 | 若不变蓝色,说明还原性:Fe2+>I— |
| 步骤4:(方法2)向试管中滴入少量10% KSCN溶液,振荡试管 | 若不变红色,说明还原性: 若变红色,说明还原性:Fe2+>I— |


科目:高中化学 来源:不详 题型:填空题
 N2O4 △H<0,根据图像判断后填空:
N2O4 △H<0,根据图像判断后填空:
|
 t1 t2 t3 t4 t5 t6 t
t1 t2 t3 t4 t5 t6 t
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 zC(g)达平衡时,A的浓度为0.5mol·L-1,若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.2 mol·L-1.下列判断正确的是
zC(g)达平衡时,A的浓度为0.5mol·L-1,若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A的浓度降为0.2 mol·L-1.下列判断正确的是| A.x+y<z | B.平衡向逆反应方向移动 |
| C.B的转化率降低 | D.C的体积分数减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.S(s)+O2(g)  SO2(g)(正反应为放热反应) SO2(g)(正反应为放热反应) |
B.N2(g) + 3H2(g)  2NH3(g)(正反应为放热反应) 2NH3(g)(正反应为放热反应) |
C.C(s)+ CO2(g)  2CO(g) (正反应为吸热反应) 2CO(g) (正反应为吸热反应) |
D.H2(g)+ I2(g) 2HI(g) (正反应为吸热反应) 2HI(g) (正反应为吸热反应) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 FeO(s)+CO(g);△H>0
FeO(s)+CO(g);△H>0
| A.升高温度 | B.增大压强 | C.充入一定量氮气 | D.再加入一些铁粉 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
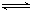 3C(g)+2D(g),(b为
3C(g)+2D(g),(b为 3的正整数) 。
3的正整数) 。 (B)= 。
(B)= 。| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3COO-+H+
CH3COO-+H+ CH3COOH+OH-
CH3COOH+OH- 3COO-),则溶液的pH为_______
3COO-),则溶液的pH为_______ (填数值)。
(填数值)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 图所示,容器A左侧是可平行移动的活塞。向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL。在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)
图所示,容器A左侧是可平行移动的活塞。向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL。在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)  Z(g)+2W(g),达到平衡时V(A)=1.2aL。试回答:
Z(g)+2W(g),达到平衡时V(A)=1.2aL。试回答:
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则关于X、Y、Z、W四种物质的聚集状态说法正确的是( )
Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则关于X、Y、Z、W四种物质的聚集状态说法正确的是( )
| A.X、Y均为气体,Z、W中有一种为气体 |
| B.Z、W中有一种是气体,X、Y皆非气体 |
| C.X、Y、Z、W皆非气体 |
| D.Z、W均为气体,X、Y中有一种是气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com