
(1)C7H16名称
(2)指出下列反应的类型乙烯使酸性高锰酸钾溶液褪色:
(3)写出反应的化学方程式:三氯甲烷与氯气在光照下反应 .
考点:
化学方程式的书写;有机化合物命名;乙烯的化学性质.
分析:
(1)该有机物为烷烃,根据烷烃的习惯命名法进行解答;
(2)高锰酸钾具有强氧化性,具有还原性的物质能被高锰酸钾氧化,从而使高锰酸钾褪色;
(3)三氯甲烷中的氢原子可以被卤素原子取代;
解答:
解:(1)该有机物含有7个C,16个氢符合烷烃的通式,所以习惯命名为庚烷,
故答案为:庚烷;
(2)乙烯具有还原性,能与具有强氧化性的酸性KMnO4溶液反应而褪色,
故答案为:氧化反应;
(3)三氯甲烷中的氢原子可以被氯原子取代,即CHCl3+Cl2 CCl4+HCl,
CCl4+HCl,
故答案为:CHCl3+Cl2 CCl4+HCl;
CCl4+HCl;
点评:
本题考查烷烃的命名、反应类型的判断、化学方程式的书写等,侧重烷烃、烯烃性质的考查,题目难度不大,旨在考查学生对基础知识的理解掌握.


科目:高中化学 来源: 题型:
央广网北京消息,据中国之声《央广新闻》报道,雾霾天气今起再次正面袭扰京津冀等地,部分地区有中到重度霾。解决环境问题需要化学知识,化学与生活联系紧密,下列说法正确的是
A.我国重点城市近年来已发布“空气质量日报”,将CO2、NO2和可吸入颗粒物等列入了首要污染物
B.PM 2.5(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶
C.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量
D.绿色化学的核心是利用化学原理对环境污染进行治理
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程属于取代反应的是( )
|
| A. | 苯与碘水混合振荡,水层颜色变浅发生萃取 |
|
| B. | 乙烯使溴水褪色 |
|
| C. | 甲烷与氯气光照下反应 |
|
| D. | 乙烯与氯化氢在一定条件下反应制取纯净的一氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A+3B=2C+2D在不同条件下反应速率如下,其中最快的是( )
|
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.6mol/(L•min) |
|
| C. | v(C)=0.4mol/(L•min) | D. | v(D)=0.0075 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案中,不能测定Na2CO3和NaHCO3,混合物中Na2CO3质量分数的是
A.取a克混合物充分加热,建中b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体。
查看答案和解析>>
科目:高中化学 来源: 题型:
是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:
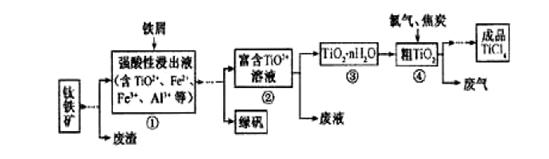
回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe === 3Fe2+
2TiO2+(无色) +Fe+4H+ === 2Ti3+(紫色) +Fe2++2H2O
Ti3+(紫色) +Fe3++H2O === TiO2+(无色) +Fe2++2H+
加入铁屑的作用是____________。
(2)在②→③工艺中需要控制条件以形成TiO2·n H2O溶胶,该分散质颗粒直径大小在_____________范围。
(3)若把③中制得的固体TiO2·n H2O用酸清洗除去其中的Fe (OH)3杂质,还可制得钛白粉。已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe (OH)3+3H+ Fe3+ +H2O的
Fe3+ +H2O的 平衡常数K=_____________。
平衡常数K=_____________。
(4)已知:TiO2 (s) +2 Cl2 (g)=== TiCl4(l) +O2(g) △H=+140KJ·mol-1
2C(s) +O2(g)=== 2CO(g) △H=—221KJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:_____________。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是_____________(只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4 ,可采用_____________方法。
| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
[实验]制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
(1)下列有关制备银镜过程的说法正确的是 。
a.边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水。至最初的沉淀恰好溶解为止
b.将几滴银氨溶液滴入2 mL乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配制过程中,溶液的pH增大
[提出假设]
假设1:Fe1+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3能氧化Ag。
[设计实验方案,验证假设]
(2)甲同学从上述实验的生成物中检验出Fe3+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式: 。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示: NO 在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① ② …… | 若银镜消失,假设2成立。 若银镜不消失,假设2不成立。 |
[思考与交流]
(4)甲同学验证了假设1成立,若乙同学验证了假设2也成立。则丙同学由此得出结论:Fe(NO3 )3溶液中的Fe3+和NO
)3溶液中的Fe3+和NO 都氧化了Ag。
都氧化了Ag。
你是否同意丙同学的结论,并简述理由: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及铁的化合物应用广泛.如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式_______________________________。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应___________________ 负极反应________________________
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤__________________________。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时约pH | |
| Fe3+ Fe2+ Cu2+ | 1.9 7.0 4.7 | 3.2 9.0 6.7 |
| 提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢。但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式__________________________
劣质不锈钢腐蚀的实验现象_________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com