
科目:高中化学 来源: 题型:
粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。通常经过以下步骤:
①加入稍过量的BaCl2溶液;
②加入稍过量的NaOH溶液;
③加入稍过量的Na2CO3溶液;
④过滤;
⑤滴入稀盐酸至无气泡产生;
回答下列问题。
(1)实验室进行NaCl溶液蒸发时,包含以下操作步骤:①固定铁圈位置;②放上蒸发皿(蒸发皿中盛有NaCl溶液);③放置酒精灯;④加热搅拌;⑤停止加热。其正确的操作顺序为________________________。
(2)如何运用最简单方法检验粗盐的提纯步骤①后溶液中有无S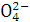 ?
?
_________________________________________________________________。
(3)步骤③加入稍过量的Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的是 ______________________________________________________________。
(4)步骤④为过滤操作。请问这一操作能除掉哪些杂质? __________________
_________________________________________________________________。
(5)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,使用玻璃棒的作用分别是: ____________________________
__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列判断正确的是( )
A.可用水来检验Na2O粉末中是否含有Na2O2
B.可用CO2来检验Na2O粉末中是否含有Na2O2
C.可利用在空气中加热的方法除去Na2O中的Na2O2
D.将足量的Na2O2、Na2O分别加到酚酞试液中,最终溶液均为红色
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润的有色布条的广口瓶,可观察到的现象是____________________________________。
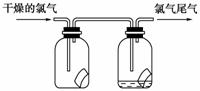
(2)为防止氯气尾气污染空气,实验室通常用________溶液吸收多余的氯气,原理是(用化学方程式表示)____________________________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是________(用字母代号填)。
A.O2 B.Cl2
C.CO2 D.HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
微波是一种高频电磁振荡波,“微波炉”就是利用高频电磁振荡使食品中分子也产生振荡而发热。现代医学上使用微波手术刀进行外科手术,其好处主要是使开刀处的血液迅速凝固而减少失血,关于其作用原理的说法正确的是( )
A.微波电流迅速中和血液胶粒所带的电荷而聚沉
B.微波使局部血液受热而使血液胶体聚沉
C.微波电流通过金属手术刀时产生的高温使血液聚沉
D.以上说法都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
有甲、乙、丙、丁四种液体,它们分别为Fe(OH)3胶体、硅酸胶体、As2S3胶体、NaOH溶液。现将有关实验现象记录如下:
①电泳:甲液体的阳极周围颜色变浅,阴极周围颜色变深。②将一束光通过乙液体,无丁达尔现象。③将乙慢慢地加入到丙溶液中,先出现凝聚,后液体变清。试推断甲为________,乙为______________,丙为____________,丁为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
超细氮化铝粉末被广泛应用于大规模集成电路生产等领域,其制取原理为Al2O3+N2+3C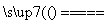 2AlN+3CO,由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质,为测定该产品中有关成分的含量,进行了以下两个实验。
2AlN+3CO,由于反应不完全,氮化铝产品中往往含有炭和氧化铝杂质,为测定该产品中有关成分的含量,进行了以下两个实验。
(1)称取10.00 g产品,将其加入过量的NaOH浓溶液中共热并蒸干,AlN跟NaOH溶液反应生成Na[Al(OH)4],并放出氨气3.36 L(标准状况)。
①上述反应的化学方程式为______________________________________________;
②计算该样品中AlN的质量分数。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
(2)另取10.00 g样品置于反应器中,通入2.016 L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34 g·L-1(已折算成标准状况,AlN不跟O2反应)。计算该样品中含杂质炭的质量。
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com