
【题目】(1)水的电离平衡曲线如下图所示。
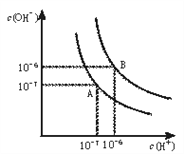
将100℃下的pH=8的Ba(OH)2溶液与100℃下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7, 则Ba(OH)2与盐酸的体积比为______________
(2)下列关于水电离的说法正确的是(____)
A.水电离是熵增加的反应,反应吸热,故能自发进行
B.升高温度水分子的活化分子数增多,有效碰撞几率减小,电离速率加快
C.向水中加入多电子体,加快H+和O2-之间的电子传递, 破坏水的电离平衡,是研究水分解的方向之一
D.水电离本质上是水分子间的氢键瞬间作用力加强造成的
【答案】 2:9 AD
【解析】(1)100℃时,Kw=10-12,pH=8的Ba(OH)2溶液中c(OH-)=10-4mol/L,pH=5的稀盐酸中c(H+)=10-5 mol/L,设氢氧化钡的体积为x,盐酸的体积为y,保持100℃的恒温,欲使混合溶液pH=7,溶液呈碱性,混合溶液中c(OH-)=![]() mol/L=10-5 mol/L,c(OH-)=
mol/L=10-5 mol/L,c(OH-)=![]() =10-5 mol/L,x:y=2:9,故答案为:2:9;
=10-5 mol/L,x:y=2:9,故答案为:2:9;
(2) A.水电离是熵增加的反应,电离过程需要吸热,即△S>0,△H>0,△G=△H-T△S,在一定温度下可以使得△G<0,能自发进行,故A正确;B.升高温度水分子的活化分子数增多,有效碰撞几率增大,电离速率加快,故B错误;C.水中不存在O2-,故C错误;D.水分子间的氢键瞬间作用力加强,使得氢氧共价键发生断裂,使水电离成氢离子和氢氧根离子,故D正确;故选AD。


科目:高中化学 来源: 题型:
【题目】下图表示几种中学常见物质之间的相互转化关系(图中部分条件或产物已省略),其中B为黑色的非金属固体单质,D可使品红溶液褪色,E在通常状况下是无色无味的液体,I在通常状况下是无色气体,G是淡黄色的固体化合物,H是黑色晶体. 
请回答下列问题:
(1)单质F的组成元素在周期表中的位置是(指明周期和族),G的电子式为 , 化合物J的俗名 .
(2)金属Al和H的混合物俗称
(3)镁条能在气体C中燃烧得到两种固体,其化学式分别是、;
(4)写出上图中下列反应的化学方程式:
①;
③;
(5)向上图中的反应⑤得到的M、N混合液中通入H2S气体,溶液变浑浊,酸性增强.请写出该过程发生反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年全国两会普及使用了“石头纸”,这是以碳酸钙为主料(内层)、聚乙烯等高分子材料为辅料(双外层)制成的,有关“石头纸”的说法错误的是( )
A.不易燃烧B.有利于保护森林C.防油不防水D.不易降解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,由加成反应引起的是( )
A. 乙烯通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色
B. 苯加入到溴水中,振荡后溴水层褪色
C. 一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成
D. 苯在一定温度、压强和催化剂的作用下和氢气反应,生成环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH- ΔH>0。下列叙述正确的是( )
H++OH- ΔH>0。下列叙述正确的是( )
A. 将水加热,Kw增大,pH不变
B. 向水中加入少量NaOH溶液,平衡逆向移动,c(OH-)减小
C. 向水中加入少量冰醋酸,平衡正向移动,c(H+)增大
D. 向水中加入少量固体NaHSO4,c(H+)增大,Kw不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指( )
A. 脱落酸 B. 甲烷 C. 生长素 D. 乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是部分短周期元素的常见化合价与原子序数的关系图: 
(1)画出元素F的原子结构示意图 .
(2)从上述元素中选取两种元素形成既含离子键又含共价键的化合物,该化合物的电子式为 .
(3)这些元素中,最高价氧化物对应的水化物中酸性最强的化合物分子式为 .
(4)C、D、G对应的简单离子半径由小到大的顺序是 . (用离子符号回答)
(5)某同学设计实验装置如图2,证明A、B、F的非金属性强弱关系:
①溶液a和溶液b分别为 , .
②溶液c中的离子反应方程式为 .
③请从原子结构的角度解释非金属性B>A的原因
(6)将1mol D2C2投入200mL 3mol/L EH3溶液中,
①转移电子的物质的量为 .
②用一个化学反应方程式表示该反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程所发生的化学变化属于取代反应的是( )
A. 在FeBr3催化作用下苯与液溴反应 B. 在镍做催化剂的条件下苯与氢气反应
C. 乙烯在空气中燃烧 D. 乙醇在铜做催化剂的条件下生成乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。

则下列热化学方程式不正确的是( )
A. 1/2A2(g)+1/2B2(g)=AB(g) ΔH=-91.5kJ·mol-1
B. A2(g)+B2(g)=2AB(g) ΔH=-183kJ·mol-1
C. 2AB(g)=A2(g)+B2(g) ΔH=+183kJ·mol-1
D. 1/2A2(g)+1/2B2=AB(g) ΔH=+91.5kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com