
| A.铁与CuSO4溶液反应后滴加KSCN溶液,溶液变红 |
| B.FeCl2既有氧化性又有还原性 |
| C.除去FeCl2溶液中的少量氯化铁,可通入氯气 |
| D.补铁保健品中,含有+3价的铁元素 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:实验题
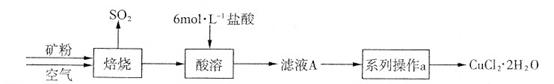
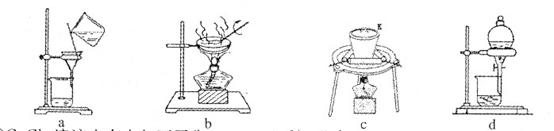
 CuCl42-(黄色)+4H2O。
CuCl42-(黄色)+4H2O。

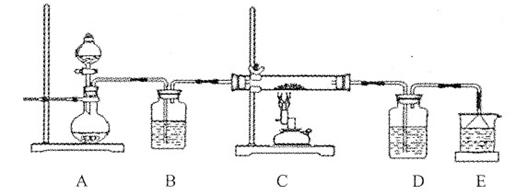
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Cu+SO2
2Cu+SO2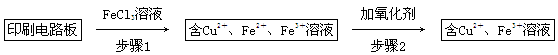
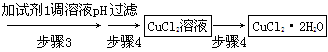
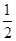 O2(g)=H2O(l) ΔH3=-286 kJ·mol-1
O2(g)=H2O(l) ΔH3=-286 kJ·mol-1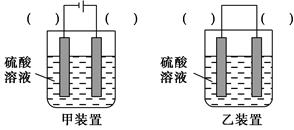
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.冶炼钢铁常采用热分解法 |
| B.Q460是含铁、碳、硅、锰、硫、磷等元素的合金钢,其中铁和锰不属于主族元素 |
| C.铝热法炼铁的反应需要高温的条件,所以是吸热反应 |
| D.增加炼铁高炉的高度可以减少尾气CO的排放 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在反应后的溶液中滴加KSCN溶液,溶液呈红色 |
| B.反应后溶液中c(Cl-)=6mol/L |
| C.反应后溶液中加入铁屑不溶解 |
| D.反应后溶液中c(Cu2+): c(Fe2+)=1:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 mol Fe分别与足量的盐酸或氯气反应电子转移数相等 |
| B.水蒸气与铁在常温下反应生成Fe3O4和H2 |
| C.Fe2O3和Al2O3都能溶解于NaOH溶液中 |
| D.生铁中的含碳量高于钢中的含碳量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com