
【题目】雾霾天气严重影响人们的生活健康,治理污染是化学工作者义不容辞的职责,因而对SO2、NOx等进行研究其有重要意义。
请根据以下信息回答有关问题:
I.NOx是汽车尾气的主要污染物之一。
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
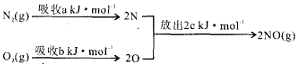
该反应的△H=__________。
(2)科学家通过实验发现,在紫外线照射下TiO2会使空气中的某些分子产生活性基团OH,并且活性基团OH可与NO2、NO发生反应生成硝酸和水。根据左下图示,请写出OH与NO反应的化学方程式__________。
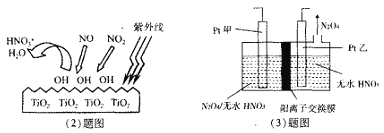
(3)电解法可将工业废气中含有的NO2消除。原理是先将NO2转化为N2O4,然后电解得到N2O5 (常温下为无色固体,常做绿色硝化剂)。电解原理如右上图所示,该电解池中生成N2O5的电极反应式是___________。
Ⅱ.工业上采取多种措施减少SO2的排放。
(4)碘循环工艺具体流程如下:
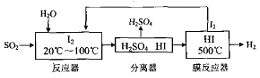
① 用化学方程式表示反应器中发生的反应___________。
② 在HI分解反应中使用膜反应器分离出H2的目的是__________。
③ 该工艺流程的优点有________。
(5)喷雾干燥法脱硫是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,吸收液中c(Ca2+)一直保持为0.70mol/L,则吸收液中的c(SO42-)为_____。[已知该温度下,Ksp (CaSO3)=1.4×10-7]
【答案】 +(a+ b-2c)kJ/mol NO+3OH =HNO3+H2O N2O4 +2HNO3-2e-=2N2O5+2H+ SO2+I2+2H2O=H2SO4+2HI HI的分解为可逆反应,分离出产物H2,有利于反应正向进行 既能吸收SO3降低污染,又能制得氢气和硫酸,反应器中生成的可以循环使用 2.0×10-7mol/L
【解析】I.(1)该反应中的反应热=反应物的键能和-生成物的键能和=(a+b)kJ/mol-2ckJ/mol=+(a+ b-2c)kJ/mol;
(2)由图象可知NO、NO2均被OH氧化为HNO3,依据原子守恒得到,NO+3OH═HNO3+H2O;
(3)N2O4制备N2O5为氧化反应,则N2O5应在阳极区生成,因此Pt甲为阳极,pt乙为阴极,阳极反应式为N2O4+2HNO3-2e-=2N2O5+2H+;
Ⅱ.(4)① 从流程图可知,在反应器中,I2氧化SO2,生成硫酸和HI,反应方程式为SO2+I2+2H2O=H2SO4+2HI;
② 因HI的分解为可逆反应,在HI分解反应中使用膜反应器分离出产物H2,有利于反应正向进行;
③ 该工艺流程的优点有既能吸收SO3降低污染,又能制得氢气和硫酸,反应器中生成的可以循环使用;
(5)C(SO32- )=![]() mol/L=2.0×10-7 mol/L。
mol/L=2.0×10-7 mol/L。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA为阿伏加德罗常数) ( )
A.124 g P4含有P—P键的个数为4NA
B.12 g石墨中含有C—C键的个数为3NA
C.12 g金刚石中含有C—C键的个数为2NA
D.60gSiO2中含Si—O键的个数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙酮(C3H60)通常是无色液体,易溶于水,密度小于1g/mL,沸点约为55℃。要从水与丙酮的混合物中将丙酮分离出来,你认为下列方法中最为合理的是( )
A.蒸馏 B.分液 C.过滤 D.蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示。其中X是原子半径最小的元素,R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物, T与Y 是同一主族元素。

(1)RX4的空间构型_____________,R在元素周期表中的位置_______________。
(2)比较X2Y、X2T稳定性强弱_________________(填化学式)
(3)判断RY2是________化合物(填“离子”或“共价”)写出RY2电子式____________,
(4)写出一个能判断R、T非金属性强弱的化学方程式________________________________。
(5)写出氯碱工业上制取Z、Y、X的离子方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型无机材料A3M4由两种非金属元素组成,元素M位于第二周期VA族。D、E、H均为难溶于水的白色固体:化合物C、E均含A元素。其余物质均为中学化学中常见物质。
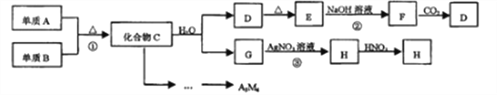
请回答:
(1)写出H的化学式:________________。
(2)化合物A3M4中含有的化学键类型为:________________。
(3)写出反应②的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000mol/L盐酸滴入20.00mL 1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是
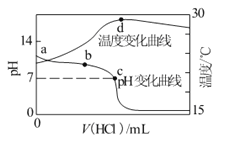
A.a点由水电离出的c(H+)=1.0×10-14molL-1
B.b点:c(NH4+)+c(NH3H2O)=c(Cl-)
C.c点:c(Cl-)=c(NH4+)
D.d点后,溶液温度略下降的主要原因是NH3H2O电离吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铁与同周期的钙性质有很大的差异,铁的熔点更高,而钙的金属活动性更强,这都说明铁的金属键比钙更_____(选填“强”、“弱”)。与钢铁比,纯净的铁有很强的抗腐蚀性,原因是_______________________。氯化铁受热会发生升华现象,这说明氯化铁是______(选填“离子”、“共价”)化合物。
(2)一定条件下,在容积一定的容器中,铁和CO2发生反应:Fe(s)+CO2(g)![]() FeO(s)+CO(g),该反应的平衡常数表达式K=_____________。下列措施中能使平衡时c(CO)/c(CO2)增大的是______(选填编号)。
FeO(s)+CO(g),该反应的平衡常数表达式K=_____________。下列措施中能使平衡时c(CO)/c(CO2)增大的是______(选填编号)。
a.升高温度 b.增大压强
c.充入一定量CO d.再加入一些铁粉
(3)FeS2可在Fe2(SO4)3溶液中“溶解”,硫元素都以SO42-形式存在,请完成该反应的化学方程式。__________
____□FeS2+ □Fe2(SO4)3 +□____→ □FeSO4 +□____
(4)溶液的酸碱性对许多物质的氧化性有很大影响;生成物的溶解性会影响复分解反应的方向。将Na2S溶液滴加到FeCl3溶液中,有单质硫生成; 将FeCl3溶液滴加到Na2S溶液中,生成的是Fe2S3而不是S或Fe(OH)3。从以上反应可得出的结论是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】收藏家收藏的清末铝制品,至今仍保存完好,其主要原因是( )
A.铝不易发生化学反应
B.铝的氧化物容易发生还原反应
C.铝不易被氧气氧化
D.铝表面致密的氧化膜能阻止铝进一步被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的H2O(g)和CO(g)分别通入到一体积为2 L的恒容密闭容器中进行反应:H2O(g)+CO(g)CO2(g)+H2(g),得到以下三组数据,据此回答下列问题:
实验组 | 温度 | 起始量 | 平衡量 | 达到平衡所需时间 | ||
H2O | CO | H2 | CO | |||
1 | 650℃ | 1 mol | 2 mol | 0.8 mol | 1.2 mol | 5 min |
2 | 900℃ | 0.5 mol | 1 mol | 0.2 mol | 0.8 mol | 3 min |
3 | 900℃ | a | b | c | d | t |
(1)①由以上数据,实验1中以v(CO2)表示反应速率为_______,以α(CO)表示转化率为_____。
②该反应在650℃时平衡常数数值为_________,该反应的逆反应为_________ (填“吸”或“放”)热反应。
③若实验3和实验2中CO的百分含量相同,且t<3 min,则a、b应满足的关系是_______。
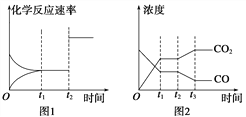
(2)下图1、2表示上述反应在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化的情况:
①图1中时刻t2发生改变的条件可能是____________(写一条即可,下同)。
②图2中时刻t2发生改变的条件可能是______________________________________。
(3)在850 ℃时,其平衡常数K=1,850 ℃时在该容器中同时充入1.0 mol CO、3.0 mol H2O、1.0 mol CO2、5.0 mol H2,此时应向________(填“正反应”或“逆反应”)方向进行,平衡时CO2的物质的量为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com