
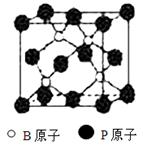


科目:高中化学 来源:不详 题型:单选题
| A.22% | B.70% | C.66.7% | D.33.3% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Zn采取六方最密堆积,空间利用率是68% |
| B.原子晶体中只含有共价键 |
| C.原子晶体的熔点一定比金属晶体的高 |
| D.离子晶体中只含有离子键,不含有共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金刚石>晶体硅>碳化硅 | B.CF4>CCl4>CBr4 |
| C.NH3>N2>H2 | D.纯镁>镁铝合金>纯铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH5属于离子晶体 |
| B.NH5属于分子晶体 |
| C.NH5与水反应时,NH5是还原剂 |
| D.NH5与NH3溶于水后均呈碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 )中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8
)中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8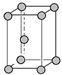 中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12
中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com