(2010?青岛二模)(1)某化学兴趣小组的同学进行Cl
2、NH
3的制备、性质等实验的流程和部分装置如下:
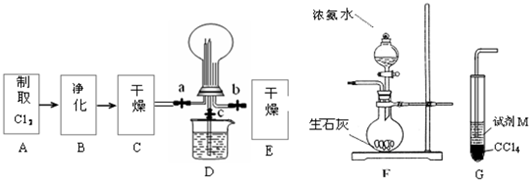
①请利用A、G装置设计一个简单的实验验证Cl
2、Fe
3+、I
2的氧化性强弱为Cl
2>Fe
3+>I
2(实验中不断小心振荡G装置中的试管).请回答A中发生反应的离子方程式
MnO
2+4H
++2Cl
- Cl
2↑+Mn
2++2H
2O
MnO
2+4H
++2Cl
- Cl
2↑+Mn
2++2H
2O
,试剂M为
FeI2
FeI2
溶液,证明氧化性为Cl
2>Fe
3+>I
2的 实验现象是
先观察到下层CCl4由无色变为紫红色,后看到上层溶液由浅绿色变为黄色;
先观察到下层CCl4由无色变为紫红色,后看到上层溶液由浅绿色变为黄色;
;
②已知3Cl
2+2NH
3=6HCl+N
2,当D的烧瓶中充满黄绿色气体后,关闭a、c打开b,D中的现象为
黄绿色气体消失,产生白烟,
黄绿色气体消失,产生白烟,
,反应一段时间后,关闭b打开c,观察到的现象为
烧杯中的液体进入烧瓶中,形成喷泉
烧杯中的液体进入烧瓶中,形成喷泉
;
③为使实验顺利进行,请简述F中的分液漏斗的正确操作方法
将F装置中分液漏斗顶端的塞子打开,再打开分液漏斗的旋塞,使分液漏斗中的液体
流下.
将F装置中分液漏斗顶端的塞子打开,再打开分液漏斗的旋塞,使分液漏斗中的液体
流下.
;
(2)某废水中含有一定量的Na
+、SO
32-,可能含有CO
32-,某研究小组欲测定其中SO
32-离子的浓度,设计如下实验方案:

①从下列试剂中选择试剂x为
C
C
(填序号):
A.0.1mol?L
-1KMnO
4(H
2SO
4酸化)溶液
B.0.5mol?L
-11NaOH溶液
C.新制氯水
D.KI溶液
②加入试剂x生成SO
42-的离子方程式为
Cl2+SO32-+H2O=2Cl-+SO42-+2H+;
Cl2+SO32-+H2O=2Cl-+SO42-+2H+;
;
③第ⅲ步的“系列操作”包含的操作名称为
过滤
过滤
、
洗涤
洗涤
、
干燥
干燥
;
④证明该废水中是否含有CO
32-的实验方案为
向废水中加入足量的盐酸,将生成的气体先通入足量的酸性KMnO4溶液,再通入澄清石灰水,若紫色KMnO4溶液颜色变浅,石灰水变浑浊,则证明废水中含有CO32-
向废水中加入足量的盐酸,将生成的气体先通入足量的酸性KMnO4溶液,再通入澄清石灰水,若紫色KMnO4溶液颜色变浅,石灰水变浑浊,则证明废水中含有CO32-
.



 小学课时特训系列答案
小学课时特训系列答案

