
【题目】下列叙述正确的是 ( )
A. 甲苯既可使溴的CCl4溶液褪色,也可使KMnO4酸性溶液褪色
B. 有机物![]() 的消去产物有2种
的消去产物有2种
C. 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2===CH—COOCH3
D. 可用溴水鉴别直馏汽油、四氯化碳和乙酸
【答案】D
【解析】A. 甲苯可以使KMnO4酸性溶液褪色,但是不能使溴的CCl4溶液褪色,A不正确;B. 有机物![]() 的消去产物只有1种,B不正确;C. 有机物A(C4H6O2)能发生加聚反应,可推知A的分子中有碳碳双键或碳碳叁键,其结构有多种可能,可能为CH2=CH—COOCH3、CH2=CH—CH2COOH、CH2=C( CH3)—COOH、CH3CH=CH—COOH、CH2(OH)C
的消去产物只有1种,B不正确;C. 有机物A(C4H6O2)能发生加聚反应,可推知A的分子中有碳碳双键或碳碳叁键,其结构有多种可能,可能为CH2=CH—COOCH3、CH2=CH—CH2COOH、CH2=C( CH3)—COOH、CH3CH=CH—COOH、CH2(OH)C![]() CCH2OH、HC
CCH2OH、HC![]() CCHOHCH2OH等等,C不正确;D. 直馏汽油中含有烯烃,故其可以使溴水褪色;四氯化碳可以把溴水中的溴萃取出来,下层变为橙红色;乙酸与溴水可以溶在一起,无明显变化。所以,可用溴水鉴别直馏汽油、四氯化碳和乙酸,D正确,本题选D。
CCHOHCH2OH等等,C不正确;D. 直馏汽油中含有烯烃,故其可以使溴水褪色;四氯化碳可以把溴水中的溴萃取出来,下层变为橙红色;乙酸与溴水可以溶在一起,无明显变化。所以,可用溴水鉴别直馏汽油、四氯化碳和乙酸,D正确,本题选D。


科目:高中化学 来源: 题型:
【题目】把煤作为燃料可通过下列两种途径:途径Ⅰ:C(s)+O2(g)=CO2(g) ΔH1<0 ①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) ΔH2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) ΔH3<0 ③
2H2(g)+O2(g)=2H2O(g) ΔH4<0 ④
请回答下列问题:
(1)途径Ⅰ放出的热量_________途径Ⅱ放出的热量。(填“>”、“=”或“<”)
(2)用ΔH2、ΔH3、ΔH4表示ΔH1的数学关系式是__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫煤燃烧会产生大气污染,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是

A.该过程中可得到化工产品H2SO4
B.该工艺流程是除去煤燃烧时产生的SO2
C.该过程中化合价发生改变的元素为Fe和S
D.图中涉及到的反应之一为Fe2(SO4)3 + SO2 + 2H2O == 2FeSO4 + 2H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为NO2、稀硝酸的还原产物为NO。实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
(1)请写出实验室中用Cu与稀HNO3反应制取NO的化学方程式并用双线桥标明电子的转移方向及数目_________________
(2)64gCu与适量的浓HNO3反应,铜全部作用后,共收集到22.4L气体(标准状况下),反应中消耗的HNO3的物质的量是_________(填字母代号)。
A.0.5mol B. 1.0mol C. 2.0mol D. 3.0mol
产生的气体分别是_______________,其物质的量之比是_______________
(3)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等,请将下列3种物质:FeSO4、Fe(NO3)3和Fe2(SO4)3分别填入下面对应的横线上,并配平该反应的化学方程式。___HNO3+_______→ _______+ _______ +___ NO↑+___H2O
(4)硝酸的还原产物NO、NO2、N2O等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念--“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质铜制取硝酸铜的方法可行且符合“绿色化学”的是_______(填字母代号)。
A.Cu![]() Cu(NO3)2
Cu(NO3)2
B.Cu![]() CuO
CuO![]() Cu(NO3)2
Cu(NO3)2
C.Cu![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2![]() Cu(NO3)2
Cu(NO3)2
D.Cu![]() CuSO4
CuSO4![]() Cu(NO3)2
Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2 L的密闭容器中发生反应:N2O4(g)![]() 2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。

(1)该温度下,该反应的平衡常数为______________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的是________点。从起点开始首次达到平衡时,以NO2表示的反应速率为____________。
(3)25 min时,加入了__________(填加入物质的化学式及加入的物质的量),使平衡发生了移动。
(4)d点对应NO2的物质的量浓度________(填“大于”、“小于”或“等于”)0.8 mol·L-1,理由是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为金属单质,下列物质相互转化如图所示:

试回答:
(1)写出B的化学式________,D的化学式_________。
(2)写出由E转变成F的化学方程式____________________________________。
(3)检验G溶液中阳离子的试剂为__,写出发生反应的离子方程式____________。
(4)某同学取B的溶液酸化后加入碘化钾淀粉溶液,在空气中放置一会儿变为蓝色,写出与上述变化过程相关的离子方程式__________________,____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中加入Na2O2后仍能大量共存的离子组是
A. NH4+、Ba2+、Cl![]() 、NO3- B. K+、AlO
、NO3- B. K+、AlO![]() 、Cl
、Cl![]() 、SO
、SO![]()
C. Ba2+、Mg2+、NO![]() 、HCO
、HCO![]() D. Na+、Cl
D. Na+、Cl![]() 、CO
、CO![]() 、SO
、SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列说法 一定正确的是( )
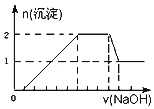
A. 一定存在H+、Mg2+、Al3+、NH4+,一定不存在Na+、SO42﹣、Fe3+
B. 一定存在H+、Al3+、NH4+、SO42﹣,可能存在Na+、Mg2+
C. 溶液中c(H+):c(Al3+):c(Mg2+)为1:1:2
D. 溶液中c(H+)/c(SO42﹣)比值小于等于2/9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多酶片中含有的蛋白酶、淀粉酶、脂肪酶具有辅助消化的作用。下列关于酶的叙述正确的是
A.多酶片中酶的基本组成单位是氨基酸
B.酶的数量因参与化学反应而减少
C.酶提供化学反应开始时所必需的活化能
D.酶在生物体内才起催化作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com