
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
 .
.分析 X、Y、Z、W是元素周期表前四周期中的四种常见元素,X的基态原子核外3个能级上有电子,且每个能级上的电子数相同,X原子核外电子排布式为1s22s22p2,则X为碳元素;常温常压下,Y单质是淡黄色固体,常在火山口附近沉积,则Y为硫元素;Z和Y同周期,Z的电负性大于Y,则Z为Cl元素;W的一种核素的质量数为63,中子数为34,则其质子数=63-34=29,则W为Cu元素,据此解答.
解答 解:X、Y、Z、W是元素周期表前四周期中的四种常见元素,X的基态原子核外3个能级上有电子,且每个能级上的电子数相同,X原子核外电子排布式为1s22s22p2,则X为碳元素;常温常压下,Y单质是淡黄色固体,常在火山口附近沉积,则Y为硫元素;Z和Y同周期,Z的电负性大于Y,则Z为Cl元素;W的一种核素的质量数为63,中子数为34,则其质子数=63-34=29,则W为Cu元素,
(1)Z为Cl元素,位于元素周期表第三周期第ⅦA族,Y为硫元素,Y的氢化物电子式是 ,故答案为:三;ⅦA;
,故答案为:三;ⅦA; ;
;
(2)CS2是一种常用的溶剂,结构与CO2类似,CS2的分子中存在2个σ键.在H-S、H-Cl两种共价键中,Cl元素的电负性更大,对键合电子的吸引力更强,故H-Cl键的极性较强,键长较长的是H-S键,对应氢化物较稳定的是HCl,
故答案为:2;H-Cl;H-S;HCl;
(3)碳与浓硫酸反应的方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(4)W为Cu元素,质子数为29,原子核外电子数为29,基态原子核外电子排布为1s22s22p63s23p63d104s1,基态原子外围电子排布式为3d104s1,
故答案为:3d104s1.
点评 本题考查结构性质位置关系、电子式、化学键、元素周期律、核外电子排布规律等,难度不大,推断元素是解题关键,注意基础知识的全面掌握.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:解答题
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
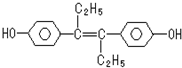
| A. | 该药物可以用有机溶剂萃取 | |
| B. | 可与NaOH反应但是不与Na2CO3发生反应 | |
| C. | 1mol该有机物不可以Br2发生取代反应 | |
| D. | 该有机物分子中,可能有16个碳原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡静置后,分液 | |
| B. | 乙醇(水):加入新制生石灰,蒸馏 | |
| C. | 溴苯(溴):加入CCl4溶液,充分振荡静置后,分液 | |
| D. | 苯中混有苯酚,加入氢氧化钠溶液,再用分液漏斗分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | Z | M | R | Q | |
| 原子半 径/nm | 0.154 | 0.074 | 0.099 | 0.143 | ||
| 主要 化合价 | -4, +4 | -2 | -1,+7 | +3 | ||
| 其他 | 阳离子核 外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60是一种新型化合物 | |
| B. | C60属于原子晶体 | |
| C. | C60在纯氧中燃烧只生成一种产物CO2 | |
| D. | C60的相对分子质量为720 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若R(OH)n为强碱,则W(OH)m也为强碱 | |
| B. | 若Y的最低负化合价为-2,则Z的最高正化合价为+6 | |
| C. | 若HnXOm为强酸,则Y是活泼非金属元素 | |
| D. | 若X的最高正化合价为+5,则五种元素一定都是非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na•+Cl:→[Na]+[•Cl:]- | B. | H2•+•O•→H:O:H | ||
| C. |  →Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-Na+ →Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-Na+ | D. |  →H:F →H:F |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com