
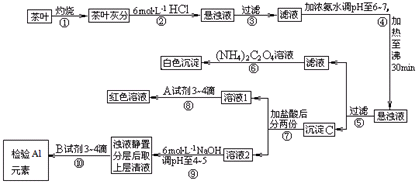
分析 茶叶经灼烧,茶叶灰中含有钙、铁、铝三种金属元素,加入盐酸后可生成可溶性的氯化物,经过滤后,在滤液中加入氨水调节pH6~7,加热至沸30min,经过滤得到的沉淀C为氢氧化铝和氢氧化铁沉淀,滤液为氯化钙溶液,加入草酸铵后可得草酸钙沉淀,在沉淀中加入盐酸后分为两份,溶液1加入试剂A,溶液变成红色,则A应为KSCN溶液,溶液2中加入6mol/L的NaOH溶液调pH至4,可得到氢氧化铁沉淀,浊液静置分层后上层清液为氯化铝溶液,加入试剂B可检验铝离子.
解答 解:茶叶经灼烧,茶叶灰中含有钙、铁、铝三种金属元素,加入盐酸后可生成可溶性的氯化物,经过滤后,在滤液中加入氨水调节pH6~7,加热至沸30min,经过滤得到的沉淀C为氢氧化铝和氢氧化铁沉淀,滤液为氯化钙溶液,加入草酸铵后可得草酸钙沉淀,在沉淀中加入盐酸后分为两份,溶液1加入试剂A,溶液变成红色,则A应为KSCN溶液,溶液2中加入6mol/L的NaOH溶液调pH至4,可得到氢氧化铁沉淀,浊液静置分层后上层清液为氯化铝溶液,加入试剂B可检验铝离子.
(1)步骤②加盐酸的作用是:使茶叶灰分中的钙、铁、铝等难溶化合物转化成可溶性氯化物 或 使Ca2+、Al3+、Fe3+浸出(或使Ca2+、Al3+、Fe3+溶解),
故答案为:使茶叶灰分中的钙、铁、铝等难溶化合物转化成可溶性氯化物 或 使Ca2+、Al3+、Fe3+浸出(或使Ca2+、Al3+、Fe3+溶解);
(2)检验Ca2+的离子方程式:Ca2++(NH4)2C2O4=CaC2O4↓+2NH4+,
故答案为:Ca2++(NH4)2C2O4=CaC2O4↓+2NH4+;
(3)步骤⑤为过滤,需要使用的主要玻璃仪器有:漏斗、烧杯、玻璃棒,
沉淀C所含主要物质的化学式:Fe(OH)3、Al(OH)3,
故答案为:漏斗、烧杯、玻璃棒;Fe(OH)3、Al(OH)3;
(4)步骤⑧用A试剂生成血红色溶液的离子方程式:Fe3++3SCN-?Fe(SCN)3,
故答案为:Fe3++3SCN-?Fe(SCN)3;
(5)步骤⑨的作用是:使Fe3+转化为Fe(OH)3沉淀,使之与铝元素分离,发生反应的离子方程式:Fe3++3OH-=Fe(OH)3↓,
故答案为:使Fe3+转化为Fe(OH)3沉淀,使之与铝元素分离;Fe3++3OH-=Fe(OH)3↓.
点评 本题考查物质性质和组成的探究实验,侧重于学生的分析和实验能力的考查,熟练掌握元素化合物性质,流程中的试剂特征和反应现象是解题关键,题目难度中等.


 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
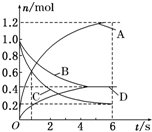 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示(6s时反应已达到平衡状态),对该反应的推断正确的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示(6s时反应已达到平衡状态),对该反应的推断正确的是( )| A. | 该反应的化学方程式为3B+4D?6A+2C | |
| B. | 反应进行到1s时,v(A)=v(C) | |
| C. | 反应进行到6s时,B和D的物质的量浓度均为0.4mol•L-1 | |
| D. | 反应进行到6s时,B的平均反应速率为0.05mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
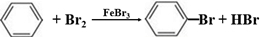
| A. | 催化剂存在条件下苯与溴反应制溴苯 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 一定条件下,乙烯与氯化氢反应制氯乙烷 | |
| D. | 光照条件下,乙烷与氯气反应制氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; ,A的二溴代物的同分异构体有3种;
,A的二溴代物的同分异构体有3种;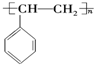 ,其单体是
,其单体是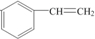 (填结构简式),写出一定条件下该单体与足量氢气反应的化学方程式
(填结构简式),写出一定条件下该单体与足量氢气反应的化学方程式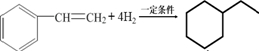 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3→Na++CO32- | B. | H2S→2H++S2- | ||
| C. | H2CO3→H++HCO3- | D. | NaHSO4→Na++H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
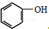 (制酚醛树脂)④
(制酚醛树脂)④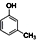 (生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料)⑥HCHO(防腐剂)
(生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料)⑥HCHO(防腐剂)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R位于第四周期ⅥA族? | |
| B. | R最高价氧化物对应的水化物的化学式为H3RO4 | |
| C. | 元素R气态氢化物的化学式为H2R | |
| D. | R的阴离子具有强还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com