
| A. | 20℃,1.01×105Pa下 11.2LN2含有的分子数为3.01×1023 | |
| B. | 4℃时9mL水和标准状况下11.2L氮气含有相同的分子数 | |
| C. | 同温同压下,lmol NO与lmol N2和O2的混合气体的体积不相等 | |
| D. | 0℃、1.01×10sPa时,11.2L氧气所含的原子数目为3.01×1023 |
分析 A.20℃,1.01×105Pa不是标准状况下;
B.4℃时9mL水的质量约为9g,根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算;
C.同温同压下气体摩尔体积相同,根据V=nVm可知二者的体积相同;
D.0℃、1.01×10sPa为标况下,11.2L氧气的物质的量为0.5mol,含有1molO原子.
解答 解:A.该条件不是标况下,不能使用标况下的气体摩尔体积计算,故A错误;
B.4℃时9mL水的质量为9g,物质的量为0.5mol,标准状况下11.2L氮气的物质的量为0.5mol,则二者含有相同的分子数,故B正确;
C.同温同压下具有相同的气体摩尔体积,则lmol NO与lmol N2和O2的混合气体的体积相等,故C错误;
D.0℃、1.01×10sPa时为标况下,11.2L氧气的物质的量为0.5mol,0.5mol氧气分子中含有1mol氧原子,所含的原子数目为6.02×1023,故D错误;
故选B.
点评 本题考查阿伏加德罗常数的计算,题目难度中等,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题培养了学生的分析能力及化学计算能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 容量瓶中原有少量蒸馏水 | |
| B. | 洗涤烧杯和玻璃棒的溶液未转入容量瓶中 | |
| C. | 定容时观察液面俯视 | |
| D. | 称量用的砝码已生锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
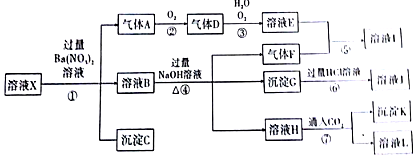
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 前4 s以N2O4的浓度变化表示的平均反应速率为0.01 mol•L-1•s-1 | |
| B. | 4 s时容器内的压强为开始时的1.2倍 | |
| C. | 平衡时容器内含0.4 mol N2O4 | |
| D. | 平衡时容器内含0.8 mol NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、SO42-、NO3- | B. | Fe3+、A13+、Cl-、HS- | ||
| C. | Na+、A1O2-、Na+、HCO3- | D. | K+、Na+、MnO4-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ③④ | C. | ①② | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁和锌分别与相同浓度的盐酸反应,镁产生H2的速率快 | |
| B. | 铜与浓硝酸反应生成NO2,与稀硝酸反应生成NO | |
| C. | 面粉加工厂内充满粉尘遇火易发生爆炸 | |
| D. | 用加热的方法可以将水中溶解的O2和N2赶出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和稀硝酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 铝与氢氧化钠溶液反应:Al+OH-═AlO2-+H2↑ | |
| C. | 醋酸跟碳酸氢钠溶液反应:HCO3-+H+═CO2↑+H2O | |
| D. | 氯气和水反应:Cl2+H2O═H++Cl-+HClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com