
把下列4种Na2S2O3溶液和相应体积的水,分别加入4个盛有20 mL 2 mol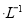 硫酸的烧杯中,此时,Na2S2O3和H2SO4缓慢地进行反应:
硫酸的烧杯中,此时,Na2S2O3和H2SO4缓慢地进行反应: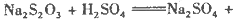
 其中最早出现明显浑浊的是
其中最早出现明显浑浊的是
A. 25 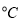 .20 mL 3 mol
.20 mL 3 mol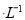 的Na2S2O3溶液,25 mL蒸馏水
的Na2S2O3溶液,25 mL蒸馏水
B. 0 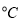 .30 mL 2 mol
.30 mL 2 mol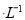 的Na2S2O3溶液,15 mL蒸馏水
的Na2S2O3溶液,15 mL蒸馏水
C.25 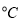 .10 mL 4 mol
.10 mL 4 mol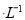 的Na2S2O3溶液,35 mL蒸馏水
的Na2S2O3溶液,35 mL蒸馏水
D.0 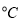 .10 mL 2mol
.10 mL 2mol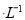 的Na2S2O3溶液,35 mL蒸馏水
的Na2S2O3溶液,35 mL蒸馏水
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源:2013-2014河南省安阳市高三毕业班第二次模拟理综化学试卷(解析版) 题型:简答题
溴化锂常用于制冷工业,可用尿素、碳酸锂及溴为原料生产溴化锂,其原理是
3Br2+3Li2CO3+CO(NH2)2 6LiBr+2H2O+N2↑+4CO2↑其主要工艺流程如下:
6LiBr+2H2O+N2↑+4CO2↑其主要工艺流程如下:
(1)溴化时,pH过小对反应不利,一方面是因为碳酸锂会反应生成_____________,另一方面使溴单质和水的反应平衡向_______移动,温度不宜超过60℃的原因是_______。
(2)反应过程中,若pH>6,产品中会有溴酸盐,其原因是BrO-发生了自身的氧化还原反应,写出反应的离子方程式:________________。
(3)试剂X的化学式为_____________,加活性炭处理的目的是________________。
(4)若直接用氨水代替尿素也可生产溴化锂,同时生成水、二氧化碳和氮气,该反应的化学方程式为_________________。
(5)用惰性电极电解熔融碳酸锂可得到金属锂,则阳极的电极方程式为______________。
(6)若原料中碳酸锂的质量为mg,最终得到溴化锂的质量为ng,据此能不能计算出溴化锂的产率?若能请写出其表达式(含m、n的表达式);若不能,请说明理由______________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高二下学期6月联考化学试卷(解析版) 题型:填空题
已知物质A分子式为C3H4O2,显酸性。F为由七个原子组成的环状结构,分子式为C6H8O4。请根据以下框图回答问题:
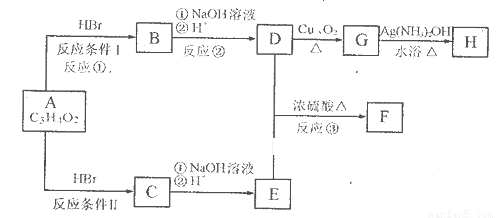
(1)A的结构简式为________________________________。
(2)反应①的反应类型为__________________________。
(3)化合物B中含氧官能团的名称是______________________________。
(4)D和E生成F的化学方程式__________________________________。
D和E按照1:1反应也可生成高聚物,请写出生成该高聚物的化学反应方程式=______
________________________________________________________________________。
(5)G生成H的化学方程式________________________________________________。
(6)写出C的同分异构体中属于酯类物质的结构简式_______________________、
________________________、____________________________________(至少写3个)
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高二下学期6月联考化学试卷(解析版) 题型:选择题
A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+与C-
C具有相同的电子层结构,下列叙述一定不正确的是
A.离子半径
B.它们的原子半径C>B>A
C.它们的原于序数A>B>C
D.原子最外层上的电子数C>A>B
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期6月联考化学试卷(解析版) 题型:填空题
(l1分)物质A-E都是中学化学中常见的物质,它们可以发生如下图所示的反应,其中E是蓝色溶液。

(1)在以上反应中(用序号填空),属于氧化还原反应的是____________,属于离子反应的是____________。
(2)写出反应③的离子方程式:____________________________________________。
(3)反应⑦的速率如上图,其原因可能是________________________________。
(4)从上述框图中选取电极材料和电解质溶液组成原电池,其中正极材料是________________________。负极反应为________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期6月联考化学试卷(解析版) 题型:选择题
已知2 mol H2(g)燃烧生成液态水放出的热量为571.6 lkJ,而2 molH2 (g)完全燃烧生成气态水放的热量为483. 6 kJ。下列说法正确的是
A. l molH2O (I)变成lmolH2O (g),向外界释放能量
B.1 molH2O (g)分解成H2(g)和O2(g),吸收241. 8 kJ能量
C.2 mol H2(g)和l mol O2(g)的总能量小于2 molH2O(1)的能量
D.断裂2 molH2O (g)中所有的O-H键,吸收483. 6 kJ能量
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省周口市高一下学期5月联考化学试卷(解析版) 题型:选择题
反应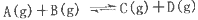 过程中的能量变化如图所示,下列说法错误的是
过程中的能量变化如图所示,下列说法错误的是

A.该反应是吸热反应
B.加入催化剂后,反应加快,A的转化率不变
C.反应物的总键能小于生成物的总键能
D.反应达到平衡时,升高温度,A的转化率增大
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省南阳市春期高一期终质量评估化学试卷(解析版) 题型:选择题
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“ · ”代表一种元素,其中O点代表氢元素.下列说法中错误的是
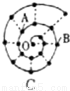
A.离O点越远的元素原子半径越大
B.虚线相连的元素处于同一族,A元素位于元素周期表ⅥA族
C.B元素是图中金属性最强的元素
D.B、C最高价氧化物的水化物可以相互反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com