
在常温下的密闭容器中充入一定量的CH4、O2和足量Na2O2,用电火花不断引燃,待反应完全后,恢复到原温度,容器内压强几乎为0。求:
(1)容器内CH4和O2的物质的量之比应为__________。
(2)若容器中Na2O2的质量为23.4 g,则容器中O2的质量m的范围为__________。
科目:高中化学 来源: 题型:
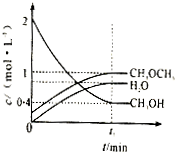 Ⅰ.(1)利用水煤气合成二甲醚(CH3OCH3)的热化学方程式为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g),△H=-274KJ/mol.该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,可以采取的措施是
Ⅰ.(1)利用水煤气合成二甲醚(CH3OCH3)的热化学方程式为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g),△H=-274KJ/mol.该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,可以采取的措施是查看答案和解析>>
科目:高中化学 来源:活题巧解巧练·高考化学(第一轮) 题型:022
在常温下的密闭容器中放入一定量的CH4,O2和足量Na2O2,用电火花不断引燃,待反应完全后,恢复到原温度,容器内压强几乎为0,求:
(1)容器内CH4和O2的物质的量之比应为________.
(2)若容器中Na2O2的质量为23.4g,则容器中O2的质量范围m为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)容器内CH4和O2的物质的量之比应为__________。
(2)若容器中Na2O2的质量为
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com