
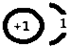
 ,D-为氯离子,它的结构示意图为:
,D-为氯离子,它的结构示意图为: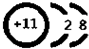 ,故答案为:
,故答案为: ,
,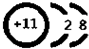 (3)B原子是氧原子,它电子式为:
(3)B原子是氧原子,它电子式为: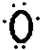 ,D-离子是氯离子,它的电子式为
,D-离子是氯离子,它的电子式为 ,故答案为:
,故答案为: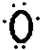 ,
, ;
;
| ||
| ||


科目:高中化学 来源: 题型:
| A、1s22s22p63s23p2 |
| B、1s22s22p63s2 |
| C、1s22s22p2 |
| D、1s22s22p63s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O和H2O2中的化学键类型完全相同 |
| B、N2的结构式为N-N |
| C、一个H2O分子所含的中子数为8(质量数:H-1,O-16) |
D、NaCl的电子式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醇在Cu或Ag的催化作用下都可以氧化成醛 |
B、有机物 的所有原子一定处于同一平面上 的所有原子一定处于同一平面上 |
| C、醇都可以在浓H2SO4作用下以及170℃时发生消去反应 |
| D、分子组成相差一个或几个CH2原子团的化合物必定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol?L-1 |

查看答案和解析>>
科目:高中化学 来源: 题型:

| 物质 | CaCO3 | MgCO3 | BaCO3 | Mg(OH)2 | Fe (OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 5.1×10-9 | 5.61×10-12 | 2.64×10-38 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com