
化学在生产和日常生活中有着重要的应用.下列说法不正确的是()
A. 铝盐(明矾溶液)和铁盐(硫酸铁溶液)都有净水作用,两者的作用原理是相同的
B. 放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
C. 0.1mol/L的CH3COONa溶液的pH约为9,说明CH3COOH是弱酸
D. 室温下向10mLpH=3的醋酸溶液中加入水稀释后,溶液中导电粒子的数目减少
考点: 盐类水解的应用;化学反应速率的影响因素;弱电解质在水溶液中的电离平衡.
分析: A、铝盐和铁盐溶液中铝离子和铁离子水解可以删除氢氧化铝、氢氧化铁胶体,胶体具有吸附悬浮杂质的作用;
B、温度降低会减小腐蚀反应的速率;
C、0.1mol/L醋酸氢离子浓度为10﹣9mol/L,说明存在电离平衡;
D、醋酸存在电离平衡,稀释促进电离氢离子物质的量增大;
解答: 解:A、铝盐和铁盐溶液中铝离子和铁离子水解可以删除氢氧化铝、氢氧化铁胶体,胶体具有吸附悬浮杂质的作用,故A正确;
B、温度降低会减小腐蚀反应的速率,放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关,故B正确;
C、0.1mol/L醋酸氢离子浓度为10﹣9mol/L,醋酸中氢离子未全部电离,说明存在电离平衡,故C正确;
D、醋酸存在电离平衡,稀释促进电离氢离子物质的量增大,溶液中导电粒子的数目增多,故D错误;
故选D.
点评: 本题材料盐类水解分析判断,弱电解质电离平衡的理解应用,掌握基础是解题关键,题目较简单.


科目:高中化学 来源: 题型:
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=﹣lgc(M),p(CO32﹣)=﹣lgc(CO32﹣).下列说法正确的是()
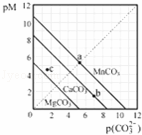
A. MgCO3、CaCO3、MnCO3的Ksp依次增大
B. a点可表示MnCO3的饱和溶液,且c(Mn2+)<c(CO32﹣)
C. b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32﹣)
D. c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
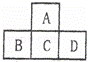
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素的原子核外共有56个电子,在周期表中的位置如图所示.E元素的最高价氧化物既能与强酸反应又能与强碱反应.请回答:
(1)写出下列元素的元素符号:A 、B 、D .
(2)A元素与氢元素形成的H2A化合物分子中,所含化学键为 键(填“离子”或“极性”或“非极性”),用电子式表示H2A的形成过程 , .
(3)A元素与E元素形成的化合物的化学式是 ,该化合物在物质分类中属于 氧化物.(填“酸性”,“碱性”或“两性”)
(4)向D元素与E元素形成的化合物的水溶液中滴加NaOH溶液,开始时,实验现象是 有 ,反应的离子方程式为 ;继续滴加NaOH溶液至过量,实验现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z为三种气体.把 a molX和 b molY充入一密闭容器中.发生反应X+2Y⇌2Z 达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为()
A. [ ]×100% B. [
]×100% B. [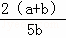 ]×100% C. [
]×100% C. [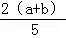 ]×100% D. [
]×100% D. [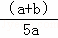 ]×100%
]×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
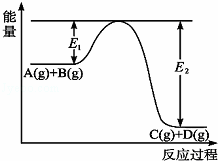
反应A(g)+B(g)⇌C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
(1)该反应是 (填“吸热”或“放热”)反应.
(2)当反应达到平衡时,升高温度,A的转化率减小(填“增大”“减小”或“不变”),原因是 .
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1 ,E2 (填“增大”“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
关于浓度均为0.1mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是()
A. c(NH+4):③>①
B. 水电离出的c(H+):②>①
C. ①和②等体积混合的溶液:c(H+)=c(OH﹣)+c(NH3•H2O)
D. ①和③等体积混合后的溶液:c(NH+4)>c(Cl﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,盐酸溶液的pH是4,氯化铵溶液的pH是5,盐酸与氯化铵溶液中水电离的c(H+)之比为()
A. 10:1 B. 1:10 C. 1:105 D. 105:1
查看答案和解析>>
科目:高中化学 来源: 题型:
禁止使用兴奋剂是奥运会保证运动员比赛公平的重要举措之一.以下两种兴奋剂结构分别为:

则关于它们的说法中正确的是( )
A. 利尿酸分子中有三种官能团
B. 两种分子中的所有碳原子均不可能共平面
C. 两种兴奋剂均属于芳香烃
D. 两种分子均可发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=﹣24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=﹣47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com