
【题目】甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的两个反应:
反应I: CO(g)+2H2(g)![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II:CO2(g)+3H2(g)![]() CH3OH(g)+ H2O(g) ΔH2
CH3OH(g)+ H2O(g) ΔH2
① 上述反应符合“原子经济”原则的是 (填“I”或“II”)。
② 下表所列数据是反应I在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为______________热反应(填“吸”或“放”)。
③ 某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从表中选择)。
(2) 已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH1 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2 kJ/mol
③H2O(g)=H2O(l) ΔH3 kJ/mol
则反应 CH3OH(l)+ O2(g)= CO(g)+ 2H2O(l) ΔH= kJ/mol
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用下图装置模拟该法:
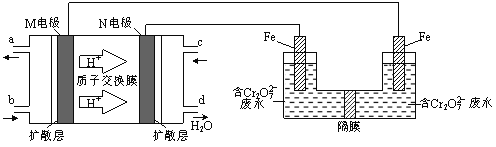
① N电极的电极反应式为 。
② 请完成电解池中Cr2O72转化为Cr3+的离子反应方程式:
Cr2O7 2+ Fe2+ + [ ] ═ Cr3++ Fe3++ [ ]
(4) 处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×105 molL﹣1 时,Cr3+沉淀完全,此时溶液的pH= 。 (已知, Ksp[Cr(OH)3]=6.4×1031,lg2=0.3)
【答案】
(1)①I(1分)②放③80%250℃
(2)(ΔH1-ΔH2+4ΔH3)/2
(3)①O2+4e+4H+=2H2O②1Cr2O27+6Fe2++14[H+]═2Cr3++6Fe3++7[H2O]
(4)5.6
【解析】
试题分析:(1)①反应I中所用原材料原子均转化到最终产物中,原子利用率为100%最经济,反应Ⅰ符合“原子经济”;
②根据表格提供的信息,温度升高,K值减小,说明平衡向逆反应方向移动,所以反应I为放热反应。
③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,物质的量为0.4mol,则CO的转化率为(2-0.4)mol÷2mol×100%=80%,K=0.8÷(0.2×1.4×1.4)=2.041,此时的温度为250℃。
(2)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)ΔH1 kJ/mol,
②2CO(g)+O2(g)=2CO2(g)ΔH2 kJ/mol,
③H2O(g)=H2O(l)ΔH3 kJ/mol,根据盖斯定律,(①﹣②+4×③)÷3可得
CH3OH(l)+O2(g)=CO(g)+2H2O(l)ΔH=(ΔH1-ΔH2+4ΔH3)/2kJ/mol。
(3)①氢离子通过质子交换膜由M电极区移向N电极区,则M为负极、N为正极,负极上发生氧化反应,甲醇失去电子,生成二氧化碳与氢离子,负极电极反应式为CH3OH﹣6e-+ H2O = 6H++ CO2↑,正极发生还原反应,氧气获得电子,与通过质子交换膜的氢离子结合为水,正极电极反应式为O2+4e+4H+=2H2O。
②电解池溶液里Cr2O72-转化为Cr3+,化合价降低共6价,左侧Fe电极为阳极,Fe失去电子生成Fe2+,酸性条件Fe2+将Cr2O72﹣还原为Cr3+,自身被氧化为Fe3+,化合价升高共1价,化合价升降最小公倍数为6,则Cr2O72﹣的系数为1,Fe2+的系数为6,反应离子方程式为Cr2O27 +6 Fe2++14H+═ 2 Cr3++6 Fe3++7H2O。
(4)Ksp=c(Cr3+)×c3(OH﹣)=6.4×1031,c(Cr3+)=1×105molL﹣1 时,溶液中c(OH﹣)=4×109molL﹣1,则c(H+)=10-14÷(4×10-9)mol/L=2.5×106molL﹣1,则pH=﹣lg2.5×106=5.6。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】己知:FeS2中S为-1价,Cu2S中S为-2价。对于反应l4CuSO4+5FeS2+12H2O =7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
A.只有硫酸铜作氧化剂
B.SO42-既不是氧化产物又不是还原产物
C.被氧化的硫与被还原的硫的质量比为3:7
D.1 mol硫酸铜可以氧化5/7 mol的硫原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
①点燃酒精灯进行加热
②在试管中加入2-3ml液体
③用试管夹夹持在试管的中上部
④将试剂瓶的瓶盖盖好,放在原处。
A. ②③④① B. ③②④① C. ②④③① D. ③②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关“电离平衡”的叙述正确的是( )
A. 电解质在溶液里达到电离平衡时,分子的浓度和离子的浓度相等
B. 电离平衡时,由于分子和离子的浓度不再发生变化,所以说电离平衡是静态平衡
C. 弱电解质达到电离平衡后,各种离子的浓度一定相等
D.电离平衡是相对的、暂时的、外界条件改变时,平衡就会发生移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氯碱工业中可以使用阴离子交换膜
B. 电解法精炼铜时,电路中每转移2mol电子,阳极质量就减少64g
C. 镀锌铁镀层破坏后锌仍能减缓铁腐蚀,其原理为牺牲阳极的阴极保护法
D. 第五套人民币的一元硬币材质为铜芯镀银,在电镀过程中,铜芯应做阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学用如图所示装置研究电化学原理。下列关于该原电池的说法不正确的是
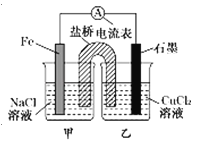
A.原电池的总反应为Fe+Cu2+═Fe2++Cu
B.盐桥中是KNO3溶液,则盐桥中NO3﹣移向乙烧杯
C.其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为2H++2e﹣═H2↑
D.反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过0.2mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨催化氧化法制硝酸的原理为4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)。在浓氨水中通入空气,将赤热铂丝插入氨水中引发反应后铂丝保持红热状态至反应停止。下列说法正确的是
4NO(g)+6H2O(g)。在浓氨水中通入空气,将赤热铂丝插入氨水中引发反应后铂丝保持红热状态至反应停止。下列说法正确的是
A.上述反应在较高温度下才能自发进行
B.该反应的正反应活化能小于逆反应活化能
C.该反应中,断裂化学键的总键能大于形成化学键的总键能
D.若NH3和O2的混合气发生上述反应,气体通入足量水中,剩余气体一定是O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质。用硼泥生产氢氧化镁的工艺流程如下图所示:
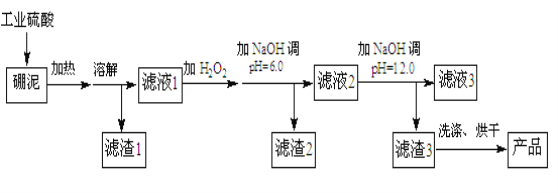
已知某些氢氧化物沉淀的pH如下表所示:
氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
Mg(OH)2 | 9.3 | 10.8 |
Fe(OH)2 | 7.6 | 9.6 |
Al(OH)3 | 4.1 | 5.4 |
Fe(OH)3 | 2.7 | 3.7 |
(1)MgO的电子式为 ,加入H2O2的目的是______________。
(2)滤渣2的主要成分是 ,向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为 。
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为 。
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为 。
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为 (用含有a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:2X(g)+Y(g) ![]() 2Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n(Z)和反应时间t的关系如右图所示,下列判断正确的是( )
2Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n(Z)和反应时间t的关系如右图所示,下列判断正确的是( )
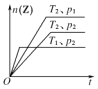
A.T1<T2,p1<p2,正反应为放热反应
B.T1>T2,p1>p2,正反应为吸热反应
C.T1>T2,p1>p2,正反应为放热反应
D.T1>T2,p1<p2,正反应为吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com