
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是

A.图中AB段的氧化剂为K2Cr2O7
B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C.开始加入的K2Cr2O7为0.25 mol
D.K2Cr2O7与FeSO4反应的物质的量之比为1∶3
科目:高中化学 来源:2016届辽宁师范大学附属中学高三上学期期中考试化学试卷(解析版) 题型:选择题
下列物质可通过化合反应一步得到的是( )
①FeCI3 ② FeCI2 ③ Fe(OH)3 ④ CuS
A.只有②③ B.只有①④ C.①②③④能得到 D.①②③能得到
查看答案和解析>>
科目:高中化学 来源:2016届广西柳州铁路第一中学高三上学期10月月考理化学试卷(解析版) 题型:推断题
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
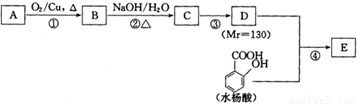
已知:2RCH2CHO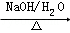
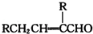
请回答下列问题:
(1)饱和一元醇A中氧的质量分数约为21.6%,则A的分子式为 。结构分析显示A只有一个甲基,则A的名称为 。
(2)B能发生银镜反应,该反应的化学方程式为 。
(3)C中含有官能团的名称为 ;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂 。
(4)第③步的反应类型为 ;D的一种同分异构体M的核磁共振氢谱显示只有一种峰,写出M的结构简式 。
(5)写出E的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江宁波效实中学高三上学期期中考试化学试卷(解析版) 题型:选择题
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源:2016届陕西西安第一中学高三上学期期中考试化学试卷(解析版) 题型:选择题
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: 。下列有关物质的推断不正确的是
。下列有关物质的推断不正确的是
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为FE,则丁可能是氯气
D.若甲为NAOH 溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高一上期中考试化学试卷(解析版) 题型:实验题
实验室用如图所示的仪器药品制取无水氯化铁粉末,已知氯化铁粉末很容易吸水生成结晶水化合物FeCl3+6H2O=FeCl3•6H2O

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序(①接_____,_____接_____,_____接_____;
(2)烧瓶A中反应方程式是 ,B中反应的化学方程式是_________。
(3)A、B中的酒精灯应先点燃 _ 处(填“A”或“B”(的酒精灯,理由是 _ 。
(4)这套实验装置是否完整? _ (填“是”或“否”(,若不完整还须补充 _ 装置(若第一问填“是”,则此问不需要作答(。
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高一上期中考试化学试卷(解析版) 题型:选择题
能够用来鉴别BaCl2、NaCl、Na2CO3三种物质的试剂是
A.AgNO3溶液 B.稀硫酸 C.稀盐酸 D.稀硝酸
查看答案和解析>>
科目:高中化学 来源:2016届北京市朝阳区高三上学期期中统考化学试卷(解析版) 题型:选择题
微电解法是利用原电池原理处理、净化高浓度有机废水的一种理想方法。在酸性、充入氧
气条件下的铁碳微电解法处理有机废水的过程中,有如下一些反应:
① O2+ 4H++4e-= 2H2O
② O2+ 2H2O+ 4e-= 4OH-
③ 4Fe2++O2+4H+= 2H2O+ 4Fe3+
......
下列有关这种铁碳微电解法处理有机废水说法不合理的是
A.在处理废水的过程中,pH升高
B.铁做负极,电极反应式是 Fe-2e-= Fe2+
C.处理、净化过程中发生的反应都是氧化还原反应
D.Fe(OH)3胶体,可净化除去废水中的悬浮物
查看答案和解析>>
科目:高中化学 来源:2016届新疆兵团农二师华山中学高三上学期第二次月考化学试卷(解析版) 题型:实验题
氯化铁是常见的水处理剂。某氯化铁(FeCl3•6H2O)样品含有少量FeCl2杂质。现要测定其中FeCl3•6H2O的质量分数,实验按以下步骤进行:

已知有关离子方程式为:2Fe3++2I-═2Fe2++I2,I2+2S2O32-═2I-+S4O62-
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻,液体呈现红褐色,反应的离子方程式为:________________________。
(2)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、_________(填仪器名称)。
(3)操作II必须用到的仪器是________(选填编号);
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
指示剂是淀粉溶液,则达到滴定终点的现象是__________________________。
(4)滴定时,消耗浓度为0.1000mol/L的标准Na2S2O3溶液18.00mL。该样品中FeCl3•6H2O(式量为270.5)的质量分数为_____________。
(5)要把样品氯化铁中的少量FeCl2杂质除去,可用的试剂是________(选填编号)。
a.铁粉 b.氯水 c.溴水 d.双氧水
(6)如果采用以下步骤测定氯化铁样品元素的含量,完成下列填空。
①称量样品 ②加水溶解 ③加足量氨水,沉淀 ④过滤 ⑤灼烧 ⑥称量并进行恒重操作。
还缺少的一步操作是________;在过滤前,需要检验是否沉淀完全,其操作___________________;判断是否恒重的标准是_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com